高血压是常见的慢性心血管疾病,是以动脉血压持续升高为特征的“心血管综合征”,是我国心脑血管病最主要的危险因素[1]。据估计,截止2025年,高血压的发病人数将超过5 亿[2]。高血压人群中大部分患者是原发性高血压,可通过抑制血管紧张素转化酶 (angiotensin I converting enzyme,简称ACE)的活性进而有效地控制血压[3]。研究表明,蛋白质通过蛋白酶的ACE 抑制肽,这类多肽可阻碍具有降血压效果的血管紧张素Ⅱ生成,同时促进缓激肽的释放,从而起到降血压的作用[4]。因此,酶法制备ACE 抑制肽成为生物活性肽研究的热点[5]。
米渣是工业上提取淀粉和糖的副产物,其蛋白质含量较高(干基约占70%)[6],富含人体必需的氨基酸,是一种优质的蛋白资源。然而,由于米渣蛋白中含有高含量的谷蛋白,此类蛋白几乎不溶于水,限制了其在食品工业中的应用,大部分作为动物性饲料或者废弃,并没有充分利用到米渣蛋白的价值。而多项研究表明,大米蛋白的酶解产物具有很强的ACE 抑制活性[7-8],若将米渣制备成活性多肽是对其的高值化利用。
目前,酶法制备多肽主要存在酶解效率低的问题,许多研究者采用新型的物理加工技术-超声波预处理将蛋白改性以后再进行酶解可显著提高蛋白的酶解效率[9-10]。在超声波的所有参数中,超声频率是影响空化效果的主要因素之一[11]。本文探讨不同超声频率对大米蛋白酶解产物的ACE抑制活性的影响,同时研究其经过胃肠消化之后活性及蛋白含量的变化,为超声辅助酶解制备大米ACE 抑制肽的领域及其进入体内后的ACE 抑制活性提供理论依据。
米渣,湖北京源山生物技术有限公司(中国湖北);碱性蛋白酶,酶活257 364.5 U/mL,诺维信有限公司(中国天津);N-[3-(2-呋喃基)丙烯酰]-L-苯丙氨酰-甘氨酰-甘氨酸 (N-[3-(2-furylacryloyl)]-L -phenyalanyl -glycyl -glycine,FAPGG),Sigma 公司;血管紧张素转化酶 (Angiotensin Iconverting enzyme,ACE),参照吴琼英等[12]的方法制备;试验中使用的所有试剂均为分析纯。
双频聚能式超声波设备,江苏大学自主研发;Tecan Infinite PRO TWIN 200 多功能酶标仪,瑞士帝肯(TECAN)集团公司;DL-5 台式离心机,上海安亭科学仪器厂;HH-S2 数显恒温水浴锅,金坛市医疗仪器厂;FD-1A-50 真空冷冻干燥,北京博医康实验仪器有限公司;PHS-3C 精密pH 计,上海精密科学仪器有限公司;Cary 100 紫外可见分光光度计,美国Varian 公司。
大米蛋白根据Yang 等[13]的方法提取,略有修改。大米蛋白质(80 g)加入到0.25%的NaOH 溶液中,50 ℃搅拌3 h 后,用1.0 mol/L 的HCl 调节上清液pH 至4.0 沉淀蛋白,然后在5 000 r/min 条件下离心15 min。将沉淀物重新悬浮于蒸馏水中,将pH 调节至7.0,将悬浮液喷雾干燥,4 ℃条件下保存,待用。
超声频率分别为单频20,35,40 和50 kHz 工作,双频同步或双频顺序20/28,20/35,20/40 和20/50 kHz 组合,设定相同的超声预处理参数:底物质量浓度50 g/L,温度30 ℃,时间15 min,间歇比5∶5,超声功率密度100 W/L。超声预处理后按照以下的酶解参数进行酶解:加酶量为5%(E/S),pH 为8,温度为50 ℃,酶解时间为90 min,酶解结束后于沸水浴条件下灭酶10 min,冷却至室温,调节pH 至7.0 后,于10 000 r/min 离心10 min,取上清液待测。
采用2.2 节同样的试验操作,酶解结束后于沸水浴条件下灭酶10 min,冷却至室温后,进行胃肠模拟消化,试验参照Ketnawa 等[14]的方法略有修改,调节酶解液的pH 值为1.5,加入2%(E/S)的胃蛋白酶,于37 ℃条件下反应2 h 模拟胃消化,反应结束后,取出于沸水浴条件下灭酶10 min,冷却后调节pH 至7.0,待测。同时以同样的方法模拟胃消化,结束后迅速调节其pH 调节至7.5,加入2%(E/S)的胰酶,于37 ℃反应4 h 模拟肠消化,反应结束后于沸水中灭酶10 min,冷却后调节pH 至7.0,离心取上清液,待测。
蛋白酶解过程中水解度的计算采用pH-stat方法[15],其计算公式如下:
式中:h——被裂解的肽键数;htot——常数,即每个底物中蛋白中含有的肽键总数,大米蛋白为8.4 mmol/g;B——消耗的碱液的体积,mL;N——碱液的浓度,mol/L;α——大米蛋白的平均解离度;m——底物中蛋白质总含量,g。
ACE 抑制活性的测定方法参照丁青芝[16]稍有修改。称取HEPES 1.910 g,NaCl 1.755 g,加适量的蒸馏水溶解,调pH 至8.3,加水定容至100 mL,4 ℃保存备用。另外称取FAPGG 19.97 mg,加HEPES 缓冲溶液溶解并定容至50 mL,4 ℃避光保存备用。样品用HEPES 缓冲液稀释100 倍,ACE用HEPES 缓冲液稀释80 倍。ACE 抑制活性的测定方法及加样顺序见表1。
表1 ACE 抑制活性的测定方法
Table 1 Determination method of ACE inhibitory activity

组分 空白孔/μL 样品孔/μL ACE 50 50 FAPGG 100 100 HEPES 缓冲液 50 0待测样品 0 50
在340 nm 波长下,分别测定对照孔和样品孔的初始吸光度(a1 和b1),37 ℃保温30 min 后再测定其吸光度(a2 和b2)。对照孔的吸光度减少值A=a1-a2,样品孔的吸光度减少值B=b1-b2。
ACE 抑制活性的计算公式为:

参考何荣海等[17] 的试验方法略有修改,取1.25 mL 样品溶液,加入2 mL 10%三氯乙酸(TCA)水溶液,混匀,静置30 min,然后在10 000 r/min 下离心10 min,将上清液全部转移到50 mL容量瓶中,用蒸馏水定容至刻度,摇匀。取6 mL 上述溶液置于试管中,加入双缩脲试剂4 mL,混匀后,静置10 min,1 000 r/min 离心10 min,取上清液于540 nm 下测定OD 值,同时以酪蛋白为标准物质制作标准曲线,与标准曲线对照得出样品溶液中的多肽浓度。
试验结果采用SPSS 13.0 软件单因素方差分析 (IBM 公司,NY,USA)P<0.05 的显著性水平下进行分析。图表采用OriginPro8(OriginLab 公司,MA,USA)绘制。
单频超声、 双频顺序超声和双频同步超声对大米蛋白DH 及酶解产物ACE 抑制活性的影响分别见图1a、图1b和图1c。由图可知,不同的超声频率对大米蛋白的DH 无显著影响 (P>0.05),但不同的超声频率对酶解产物ACE 抑制活性均具有显著影响(P<0.05)。由图1a可知,在单频超声频率为20 kHz 条件下达到最大值,与对照组相比,ACE 抑制活性提高了35.68%。图1b和c的结果表明,在20/35 kHz 组合双频顺序的条件下,蛋白酶解产物的ACE 抑制活性最大,相比于对照组,蛋白酶解产物的ACE 抑制活性提高了66.24%,与单频20 kHz 超声相比,其对酶解产物的ACE抑制活性提高了22.52%。双频20/35 kHz 同步超声较其他超声顺序超声频率提高酶解产物ACE抑制活性幅度大,相比于对照提高了56.17%,相比于单频20 kHz 超声来说,提高了15.10%。
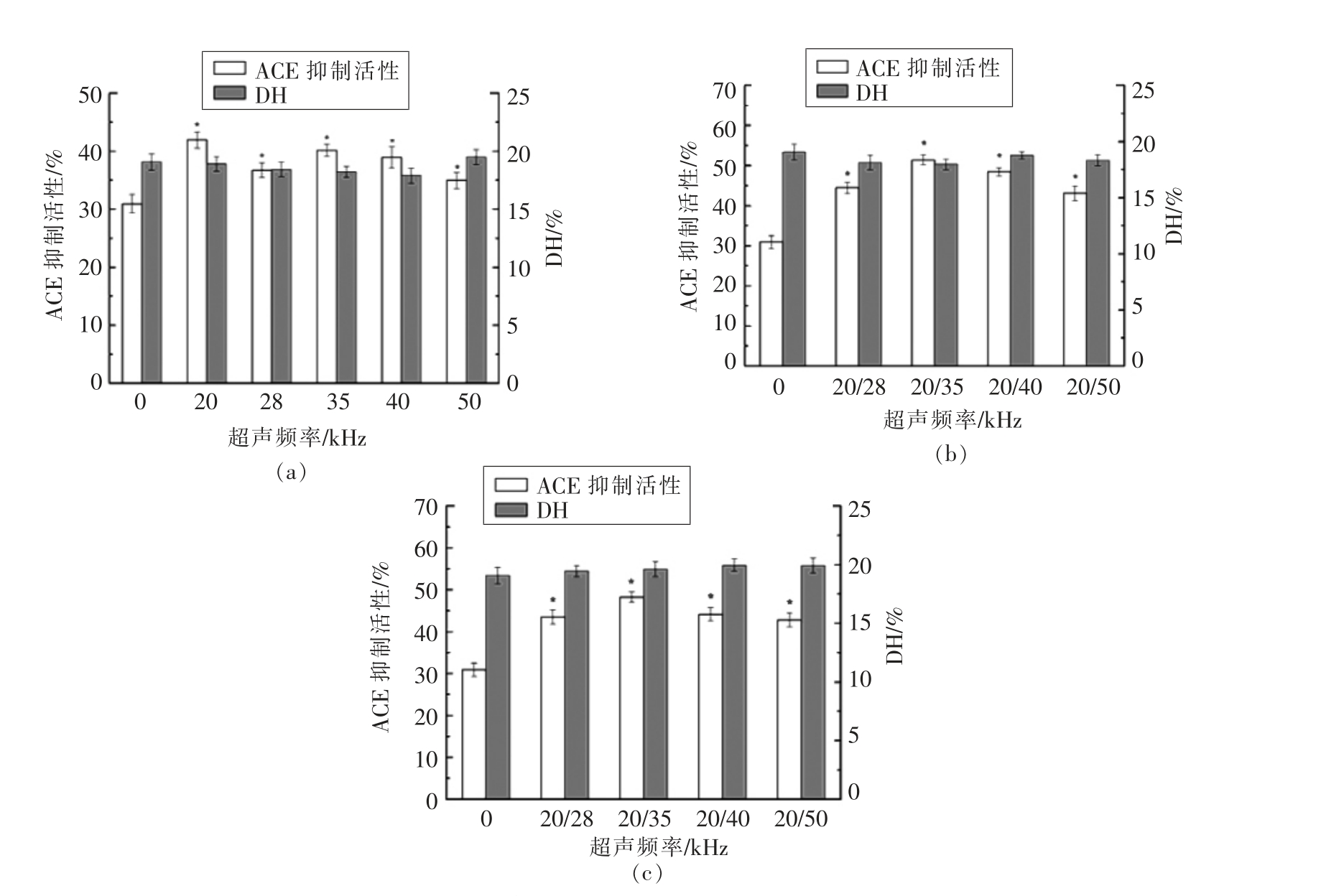
图1 单频(a)、双频顺序(b)及双频同步(c)超声对大米蛋白水解度及酶解产物ACE 抑制活性的影响
Fig.1 Effect of single-frequency(a),dual-frequency sequential (b)and dual-frequency simultaneous(c)ultrasound on DH of rice protein and ACE inhibitory activity of hydrolysate from rice protein
不同的超声频率均可显著提高酶解产物的ACE 抑制活性,这是由于天然的大米蛋白构象存在缺陷,使得其蛋白结构不适于蛋白酶解,超声波预处理改变了蛋白的分子构象,从而改变了大米蛋白的酶解特性,使得更多的与降血压活性有关的活性基团暴露。本试验的研究结果表明,双频作用效果明显优于单频作用效果,原因是双频超声组合提供了一个更宽的频谱作用范围,其对声化学反应产额的提高具有明显的增强效应[18-19]。
在相同的功率消耗下,双频顺序超声对大米蛋白酶解产物ACE 抑制活性的增强效果显著优于同步工作的效果。产生这种现象的原因可能是由于:在双频同步超声条件下,两列不同频率的超声波在同步传播时有可能在某些传播位置或相位发生波的干扰,可能会形成抵消的现象,而双频顺序工作的两种不同频率的超声波,可以对蛋白原料的不同作用靶点,提供间歇式攻击,不存在抵消的现象[20]。
单频超声、 双频顺序超声和双频同步超声对大米蛋白酶解液的胃肠模拟消化产物的ACE 率的影响分别见图2a、图2b和图2c。由图可知,经过胃肠模拟消化,单频、双频同步、双频顺序超声均能显著提高酶解产物的ACE 抑制活性(P<0.05),单频20 kHz、20/35 kHz 顺序超声和20/23 kHz 同步超声预处理后的大米蛋白酶解液的胃肠模拟消化产物的ACE 抑制活性最高,相比于对照组来说,蛋白酶解物的ACE 抑制活性经过胃消化后,分别增加了43.54%,59.16%和50.38%,经过肠消化后,分别增加了19.83%,34.52%,24.82%。
有研究表明,大豆分离蛋白经过体外模拟消化后可产生ACE 抑制肽[21],煮熟的鸡蛋经过胃肠道消化液具备ACE 抑制活性[22]。因此,胃肠道消化酶是制备ACE 抑制肽的常用蛋白酶。经过胃蛋白酶消化以后,超声能显著提高大米蛋白酶解液的ACE 抑制活性,且超声提高的幅度高于未超声,说明超声能提高胃消化阶段酶解产物的ACE 抑制活性。与胃消化相比,蛋白酶解物经过肠消化以后的ACE 抑制活性反而有所降低。
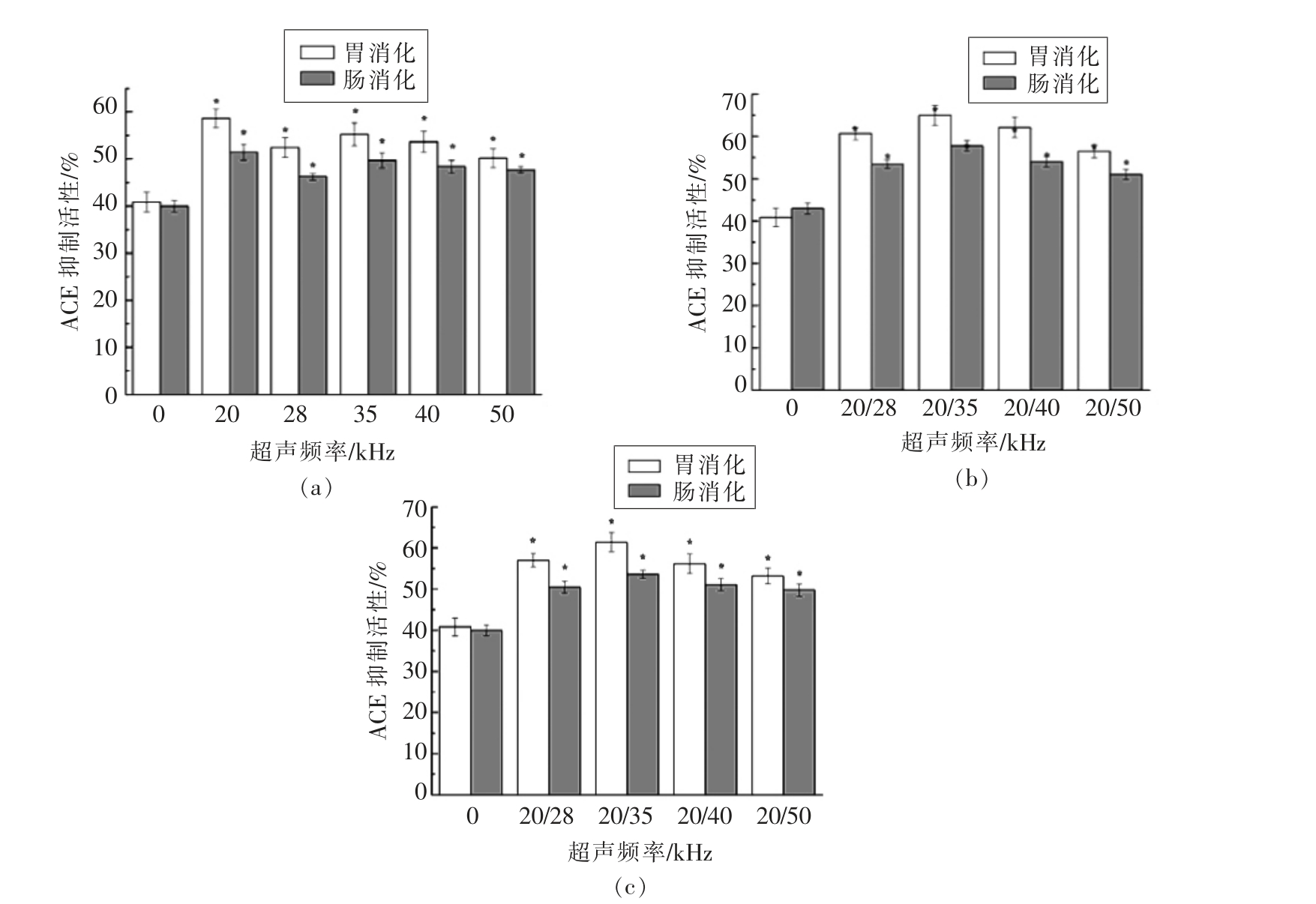
图2 单频(a)、双频顺序(b)及双频同步(c)超声对大米蛋白酶解液胃肠模拟消化产物ACE 抑制活性的影响
Fig.2 Effect of single-frequency (a),dual-frequency sequential (b)and dual-frequency simultaneous (c)ultrasound on ACE inhibitory activity of gastrointestinal simulated digestive products from rice protein hydrolysate
由以上结果可以看出,超声对大米蛋白不同阶段的酶解产物的ACE 抑制活性具有不同的影响,超声可显著提高酶解产物及胃模拟消化产物的ACE 抑制活性,而对于肠消化产物的ACE 抑制活性有所下降。原因可能与胰酶所含蛋白酶种类多,酶切位点较多,导致多肽过度降解,而形成大量无明显生物学活性的氨基酸有关。
单频超声、双频顺序超声、双频同步超声对大米蛋白酶解液及胃肠模拟消化产物的多肽含量的影响分别见图3a、图3b和图3c。由图可知,胃消化后的多肽含量显著高于未经过消化的多肽含量(P<0.05),而经过肠消化的多肽含量均低于经过胃消化的多肽含量。说明经过胃消化,胃蛋白酶将酶解液中的蛋白或长链多肽切割为小片段的多肽,而经过胰酶酶解,多肽因过度酶解而形成了部分氨基酸,导致多肽含量的降低,而使得ACE 抑制活性降低。
与未超声相比,超声可显著提高碱性蛋白酶酶解产物的多肽含量(P<0.05),从而提高了酶解产物的ACE 抑制活性,再经过胃蛋白酶消化,其多肽含量进一步增加,ACE 抑制活性也大幅度提升,由此可知,超声可显著提高碱性蛋白酶酶解产物、胃消化产物的多肽含量及ACE 抑制活性。天然的蛋白结构不利于碱性蛋白酶及胃蛋白酶的酶解,因此,超声预处理可以促进天然的蛋白结构的伸展,使得蛋白酶与底物接触的概率增加,大大提高了酶解产物的多肽含量及ACE 抑制活性。然而,酶解产物经过肠消化后,蛋白含量反而降低,原因是多肽过度酶解,形成了大量的氨基酸,使得ACE 抑制活性降低。因此,若考虑胃肠消化作用,则说明蛋白在碱性蛋白酶酶解的阶段存在过度降解,导致再经过胃和肠道的两次消化以后,反而又出现降低的趋势。因此,若充分利用胃肠的消化功能,可通过调节在体外(本文为碱性蛋白酶的酶解过程)酶解的程度,使酶解物在肠消化以后,产物的ACE 抑制活性和多肽含量达到最大值。
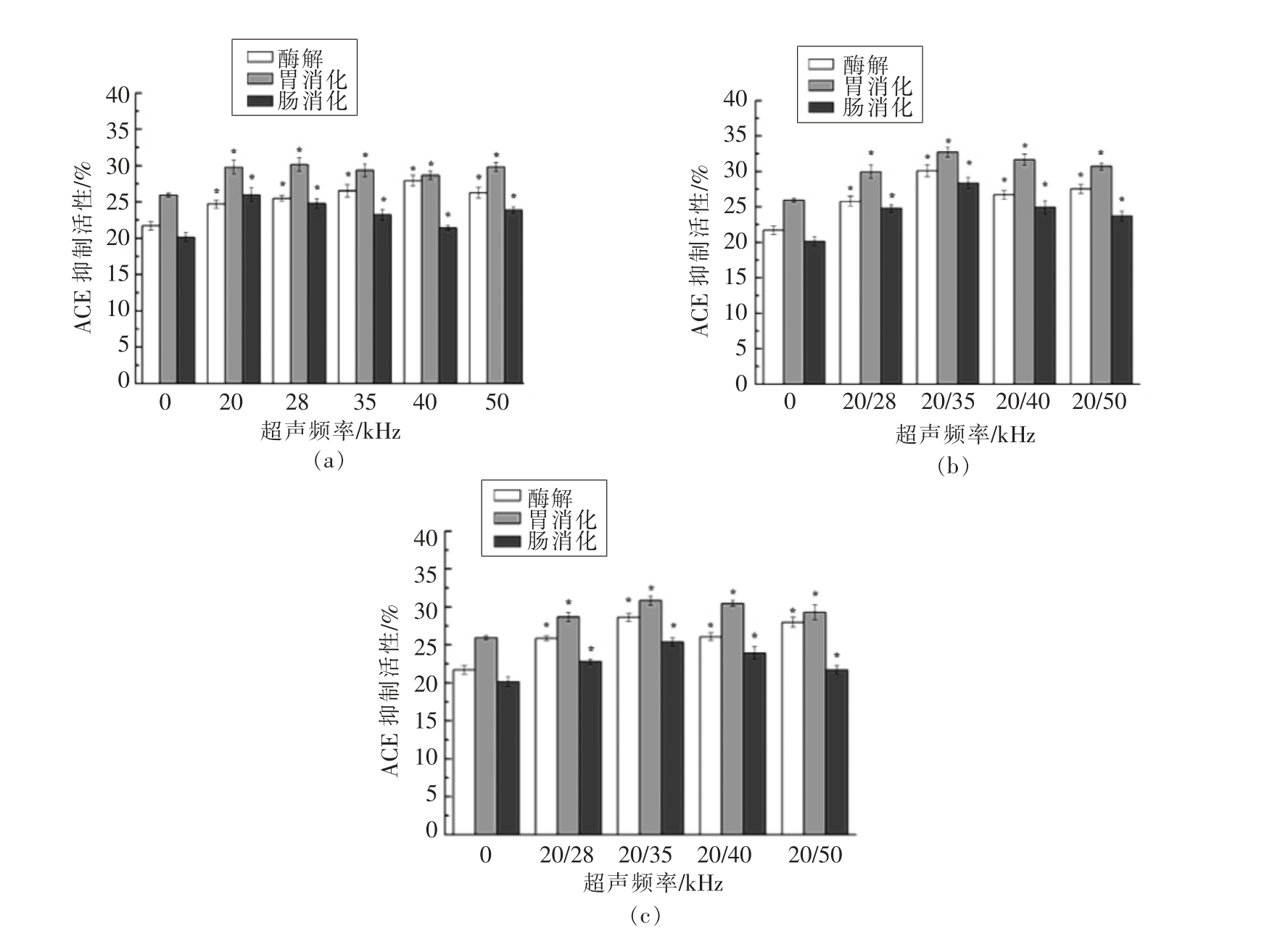
图3 单频(a)、双频顺序(b)及双频同步(c)超声对大米蛋白酶解液及胃肠模拟消化产物多肽含量的影响
Fig.3 Effect of single-frequency (a),dual-frequency sequential (b)and dual-frequency simultaneous (c)ultrasound on the peptide content of rice protein hydrolysate and gastrointestinal simulated digestive product
本文研究了不同的超声频率预处理大米蛋白对碱性蛋白酶酶解产物以及胃肠道模拟消化产物的ACE 抑制活性的影响,以及不同阶段大米蛋白酶解产物的多肽含量。主要结论如下:
1)相同的功率消耗下,不同超声频率显著提高大米蛋白酶解产物的ACE 抑制活性,双频超声较单频超声更能提高大米蛋白酶解产物的ACE抑制活性,并且双频顺序超声对酶解产物ACE 抑制活性的增强效果显著优于同步超声的效果;
2)通过超声辅助酶解大米蛋白制备ACE 抑制肽的研究,发现适合大米蛋白酶解制备ACE 抑制肽的超声波频率为20 kHz 和20/35 kHz;
3)超声预处理的大米蛋白酶解产物经过胃肠模拟消化后,其ACE 抑制活性和多肽含量均呈现出在胃消化后升高,而肠消化后降低的变化趋势。
[1]中国高血压基层管理指南 (2014年修订版)[J].中华高血压杂志,2015,23(1):24-25.
[2]IBRAHIM M M,DAMASCENO A.Hypertension in developing countries[J].The Lancet,2012,380(9841):611-619.
[3]石艳军,金义鑫,袁琳,等.食品蛋白质中血管紧张素转化酶抑制肽的研究[J].生物技术通报,2004,(6):6-10.
[4]ONDETTI M A,RUBIN B,CUSHMAN D W.Design of specific inhibitors of angiotensin-converting enzyme:new class of orally active antihypertensive agents[J].Science,1977,196(4288):441-444.
[5]赵伟睿,马海乐,贾俊强,等.超声波对麦胚蛋白性质及其酶解物ACE 抑制活性的影响[J].食品与生物技术学报,2010,29(2):177-182.
[6]贾俊强,马海乐,曲文娟,等.超声预处理大米蛋白制备抗氧化肽[J].农业工程学报,2008,24(8):288-293.
[7]马海乐,郝志伟,何荣海,等.基于超声预处理的大米降血压多肽的制备及其功能评价[J].中国食品学报,2010,10(6):36-40.
[8]陈倩倩,佟立涛,钟葵,等.大米蛋白酶解物的ACE 抑制活性研究[J].现代食品科技,2015,31(3):91-96.
[9]QU W,MA H,JIA J,et al.Enzymolysis kinetics and activities of ACE inhibitory peptides from wheat germ protein prepared with SFP ultrasound-assisted processing[J].Ultrasonics Sonochemistry,2012,19(5):1021-1026.
[10]JAIN S,ANAL A K.Optimization of extraction of functional protein hydrolysates from chicken egg shell membrane(ESM)by ultrasonic assisted extraction (UAE)and enzymatic hydrolysis[J].LWT-Food Science and Technology,2016,69:295-302.
[11]LEIGHTON T G.Bubble population phenomena in acoustic cavitation[J].Ultrasonics Sonochemistry,1995,2(2):123-136.
[12]吴琼英,马海乐,崔恒林,等.猪肺血管紧张素转化酶的提取纯化及其性质研究[J].食品科学,2004,25(9):71-74.
[13]YANG L,CHEN J,XU T,et al.Rice protein extracted by different methods affects cholesterol metabolism in rats due to its lower digestibility[J].International Journal of Molecular Sciences,2011,12:7594-7608.
[14]KETNAWA S,MARTÍNEZ -ALVAREZ O,BENJAKUL S,et al.Gelatin hydrolysates from farmed Giant catfish skin using alkaline proteases and its antioxidative function of simulated gastro-intestinal digestion[J].Food Chemistry,2016,192:34-42.
[15]ADLER-NISSEN J.Enzymic hydrolysis of food proteins[J].Elsevier Applied Science Publishers,1986:122-144.
[16]丁青芝.脉冲超声辅助酶解法制备玉米黄粉ACEI 活性肽的研究[D].镇江:江苏大学,2008.
[17]何荣海,刘磊,蒋边,等.枯草芽孢杆菌液态发酵菜籽粕制备抗氧化肽[J].中国食品学报,2013,13(12):12-20.
[18]SCHOELLHAMMER C M,SRINIVASAN S,BARMAN R,et al.Applicability and safety of dual-frequency ultrasonic treatment for the transdermal delivery of drugs[J].Journal of Controlled Release,2015,202:93-100.
[19]RAHIMI M,SAFARI S,FARYADI M,et al.Experimental investigation on proper use of dual highlow frequency ultrasound waves-Advantage and disadvantage[J].Chemical Engineering & Processing Process Intensification,2014,78(4):17-26.
[20]FENG R,ZHAO Y,ZHU C,et al.Enhancement of ultrasonic cavitation yield by multi -frequency sonication [J].Ultrasonics Sonochemistry,2002,9(5):231-236.
[21]WENDY M Y LO,EUNICE C Y LC.Angiotensin I converting enzyme Inhibitory peptides from In vitro pepsin-pancreatin digestion of soy protein[J].Journal of Agriculture and Food Chemistry,2005,53(9):3369-3376.
[22]MAJUMDER K,WU J.Angiotensin I converting enzyme inhibitory peptides from simulated in vitro gastrointestinal digestion of cooked eggs[J].Journal of Agriculture and Food Chemistry,2009,57 (2):471-477.
Effects of Ultrasonic Frequencies on ACE Inhibitory Activity of Hydrolysate and Gastrointestinal Simulated Digestive Products from Rice Protein