
高静压(High hydrostatic pressure,HHP)技术是指在室温或温和条件下实施100~2 000 MPa 下的压力处理,达到杀菌或加工食物原料的目的。HHP 处理使食品自身体积减小,即在生物体高分子的立体结构中发生氢键结合、 离子结合和疏水结合,其结果不仅影响生物细胞形态,还能改变生物高分子立体结构,引起蛋白质、酶等失活,从而成为非热杀菌的手段之一[1];HHP 对维生素、色素和风味物质等低分子化合物的共价键无明显影响,可用来改善食品的组织结构或生成新型食品。HHP 技术能够在不加热或不添加化学防腐剂的条件下保证食品安全,并能显著延长食品的冷藏期和货架期,所得加工产品的质量是传统加工产品无法媲美的,为生产高附加值的产品提供了很好的技术手段[2]。
糊化过程可分为3 个阶段:①淀粉在水中加热逐渐升温,水分子由淀粉孔隙进入淀粉颗粒内部的无定形区域[3],淀粉通过氢键作用结合部分水分子而分散,体积膨胀较小;②水温继续上升,达到开始糊化温度时,淀粉粒的周边迅速扩展,大量吸水,偏光十字消失,淀粉分子间的氢键破坏,无定形区的膨胀施压给支链淀粉结晶区致其瓦解[4],结晶区氢键开始裂解,淀粉的双螺旋结构开始松解,向单螺旋转变,再舒展成无规线团状[5-6],其后颗粒继续膨胀至网状结构,直链淀粉从网状间隙中渗漏出来,包裹着充分水化的淀粉颗粒;③继续加热,极限膨胀的颗粒开始破碎支解,支链淀粉暴露出来,淀粉体系黏度增加,最终形成胶状分散物。糊化过程是淀粉粒晶体区熔化,分子水解,颗粒不可逆膨胀过程。
糊化的淀粉分子处于无序的高能态,分子间势能的作用,使淀粉分子趋于有序重排,结晶又重新趋向平行排列,形成具有结晶结构的白色凝沉物,称为重结晶。淀粉的重结晶作用,使食品的质构与消化性发生变化,例如米饭的回生、面包与糕饼的硬化。抑制重结晶是改善食品口感、延长货架期的重要因素。当然,在某些食品的制作过程中,为达到良好的造型和食用指标,又需加强与加速重结晶,如米线、粉丝的制作[7]。
目前,HHP 对淀粉的重结晶还没有系统的研究报道,大多只是局限在示差扫描量热仪(Differential scanning calorimetry,DSC)法对重结晶性质的研究:例如高压糊化淀粉比热糊化淀粉的重结晶速度慢[8]。高压处理后玉米和小麦淀粉的老化性质与贮藏温度及淀粉来源有关[9-10]。目前高静压糊化淀粉的重结晶很多方面都是空白,例如:HHP重结晶淀粉的分子结构变化、热焓转变、颗粒形态及其宏观性质都不清晰;高静压力、水分含量、贮存时间及贮存温度对结构变化的推动作用无人问津。只有完全掌握HHP 淀粉重结晶的特性及变化规律,HHP 淀粉才能得到广泛和有效的利用。
木薯淀粉(C-型,17%链淀粉)由广西武鸣安宁淀粉有限公司提供,水分含量为6.74%,蛋白质含量为0.62%,灰分含量为0.68%。
HHP 设备型号HHP-750,由包头科发高压科技有限公司研制,传压介质为蒸馏水,最大工作压力是600 MPa;扫描电镜 (Scanning electron microscope,EM,S-3400N,HITACHI,Japan),日 立 公司;激光粒度分析仪(LS230),美国贝克曼库尔特有限公司;X-射线衍射仪 (X-ray diffraction,XRD-6000 型),日本岛津公司;快速黏度分析仪(Rapid viscosity analyzer,RVA),澳大利亚Newport scientific 仪器公司;核磁共振成像仪(PQ001),纽迈公司;傅里叶红外光谱仪(Fourier transform infrared,FTIR,Spectrum 400),美国珀金埃尔默公司(Perkin Elmer);动态流变仪,上海思尔达科学仪器公司。
木薯淀粉用蒸馏水配制成淀粉与水的溶度为30%。室温条件下搅拌均匀后装入聚乙烯袋中,真空封口。样品放入HHP 处理釜中高压处理。压力水平600 MPa,保压时间30 min。此条件的选择是根据前期研究发现该条件下木薯淀粉完全糊化[11],所得的样品分别放置25 ℃恒温培养箱及4 ℃冷藏箱进行重结晶试验,分别在2,3,4,6,8,40 d 进行取样测试。
将双面胶带贴于扫描电子显微镜的载物台上,用牙签粘取少量的样品,轻轻的在双面胶上涂抹均匀,用吸耳球吹去多余的淀粉样品,放入表面处理机中,用离子溅射镀膜仪喷碳镀金2 h,将载物台取出,放入扫描电子显微镜中进行观察,拍摄具有代表性的淀粉颗粒形貌并拍照。电子枪加速电压为2 kV,以减少对淀粉颗粒的破坏。
将0.1 g 淀粉溶于5 mL 无水乙醇中,振荡10 min 使淀粉颗粒分散均匀,并用无水乙醇做分散剂,按照仪器提示加入所需量的样品数滴,样品加入后在仪器中进行分散,在转速为1 800 r/min 条件下测定淀粉颗粒的粒度分布和颗粒的平均直径,每个样品重复测定3 次。
XRD 是利用晶体形成的X-射线衍射,对物质进行内部原子在空间分布状况的结构分析方法。将具有一定波长的X-射线照射到结晶性物质上时,由于晶体是由原子规则排列成的晶胞组成,这些规则排列的原子间距离与入射X-射线波长有相同的数量级,导致不同原子散射的X-射线相互干涉。衍射线的方向取决于晶胞的大小和形状,强度由晶胞中原子的分布决定[12]。
淀粉结晶中的原子是周期性排列的,这些原子所产生的次级X-射线发生相互的干涉作用,使次级X-射线相互叠加或抵消,形成淀粉的衍射图。由于X-射线的照射角为θ 时,衍射X-射线与照射X-射线之间成2θ 角,因此试样与记数管各自以θ 和2θ 的角速率旋转,用测角器捕捉衍射X-射线的强度(每秒计数),可以得到以衍射角为横轴,以衍射X-射线的强度为纵轴的X-衍射图[13]。
晶体X-射线衍射的基本理论是Bragg 方程(1)和Schrrer 方程(2)。

式中d——晶面间距 (Å);D——晶粒线度大小(Å);n——反射次数;θ——入射角与晶体平面之间的角度;λ——X-射线的波长(Å);β——晶体衍射峰的半高宽。当晶体线度大、晶面完整,在X-射线衍射图上出现峰宽窄、 峰尖非常尖锐的衍射峰。当晶体线度很小或晶体残缺时,晶峰则会宽化,表现为与非晶体相同的弥散衍射特征,称为结晶弥散衍射[14]。
非晶X-射线衍射的基本理论是改正后的Bragg 方程(3)和Schrrer 方程(4)
式中d——相邻分子和原子间的平均距离(Å);rm——非晶短程有序范围的大小(Å);θ——Bragg 角;λ——X-射线的波长(Å);B--非晶衍射峰的半高宽。由准Bragg 方程中可以看出,当非晶物质相邻分子间的平均距离改变时,对应衍射峰的位置将发生移动。在衍射角为0~90°的范围内,当分子间的平均距离增大时,对应的非晶峰的位置向衍射角减小的方向移动;相反,则向衍射角增大的方向移动。非晶物质在结构上只有短程有序,而无长程有序。对于同种类型的非晶体,可能成分和性质差别很大,但是它们的非晶衍射峰的形状几乎一致[15-16]。
XRD 的分析条件:特征射线CuKa,石墨单色器,管压40 kV,电流30 mA,测量角度范围2θ 为4°~40°,发射及防反射狭缝1°,接收狭缝为0.3 mm,扫描速度1.5°/min,步宽0.05°。为了避免不同样品相对水分含量差异对相对结晶强度的误差,测量前应先将淀粉样品在室温下置于相对湿度100%的干燥皿中平衡。采用MDI Jade 软件计算相对结晶度(RC)。
低场核磁共振被广泛应用于生物体系中结合水的研究,一方面因为它对被检测物无破坏性,另一方面它可以测定能反映水分子流动性的氢核的纵向弛豫时间(原子核从激化状态回复到平衡排列状态的过程叫弛豫过程,其所需的时间叫弛豫时间)T1 和横向弛豫时间T2。当水和底物紧密结合时,它就高度地固定,T2 会降低;而游离水流动性好,有较大的T2。从而得知水分结合的方式及程度。
淀粉具有特定的水分含量,而且以适当的数量、定位、定向地存在于淀粉颗粒中。水分子结合能力和流动性对淀粉的流变性质、 稳定性及其质构、外观以及对腐败的敏感性有很大的影响。淀粉质原料和产品在加工、贮藏和运输等过程中,其内部的水分含量和分布状态经常会发生改变,这也是导致原料稳定性下降、 产品品质降低的主要原因之一。
磁场强度0.5 T,线圈直径15 mm,频率21.961 MHz,温度31.99~32.00 ℃。试验前,淀粉样品经烘干,粉碎,过200 目筛后,装入15 mm 玻璃试管即可测试。
FTIR 分析法是根据分子内部原子间的相对振动及分子转动,确定物质分子结构和鉴别化合物。将一束连续波长的红外光照射试验样品,如果试验样品某个基团的振动频率或转动频率和红外光的频率一样时,分子便吸收能量,由基态跃迁到能量较高的振(转)动能级,该波长的光就被试验样品吸收并记录,得到红外光谱图。因此红外光谱图提供了许多关于官能团的信息,可以据此确定试验样品的分子类型及结构。
FTIR 以KBr 薄片为背景,采用溴化钾(KBr)压片法对不同淀粉样品进行扫描测定。为了消除水分子对吸收峰的干扰,试验前将淀粉样品和KBr 粉末分别置于105 ℃下烘干3~4 h。且将淀粉样品及溴化钾粉末在红外灯的照射下,置于玛瑙研钵中研磨10 min。试验准确称取2 mg 淀粉样品及150 mg 溴化钾粉末充分混合,将混合好的粉末倒在硫酸纸上灌注于压片机中,并抽真空2 min,以免混入空气影响样品薄片的透明度。缓慢加压至10 t,保持3 min,切断真空,缓慢除去压力,取出样品薄片,放入样品架上进行扫描,扫描波数为400~4 000 cm-1,分辨率为4 cm-1,并绘出红外光谱图。
根据AACC76-21 方法:准确称取3 g 淀粉,加入25 mL 蒸馏水,混合于RVA 专用盒内调成一定浓度的淀粉乳,采用升温-降温循环:保持50 ℃1 min;3.75 min 内加热到95 ℃;在95 ℃保持2.5 min,在3.75 min 内降到50 ℃,然后在50 ℃保持2 min,测得糊黏度曲线,分析峰值黏度PV(Peak viscosity)、谷值TV(Trough viscosity)、崩解值BD(Breakdown)、最终黏度FV(Final viscosity)、回生值SB(Setback)、峰值时间Pt(Peaking time)及成糊温度PT(Pasting temperature),每个样品重复测定3 次。
2.7.1 淀粉糊动态流变学行为测定 准确称取2.0 g 淀粉,加入25 mL 蒸馏水,配成8%的淀粉乳。用吸管将淀粉糊放入流变仪测定平台。测定选用40 mm、2°的锥板,设置间隙为0.05 mm,启动流变仪使平板进入设置间隙,吸去平板外多余淀粉糊。选择temperature ramp 测试程序,温度变化程序为:从20 ℃到95 ℃程序升温使淀粉体系糊化,然后程序降温到25 ℃测定淀粉冷却过程中的凝胶特性变化,升温速率均为4 ℃/min,降温速率为5 ℃/min,剪切速率(shear rate)为200 s-1。将流变仪温度设为25 ℃,将由糊化得到的淀粉凝胶进行应力扫描,样品采用振荡模式(frequency sweep)测定糊化以后的淀粉凝胶的黏弹性随剪切应力的变化:频率扫描范围为0.1~100 rad/s,固定应力为0.5%,温度保持在25 ℃,间隙设置为0.05 mm,夹具仍使用40 mm、2°的锥板。
2.7.2 淀粉糊的剪切稀化测定 将糊化得到的淀粉凝胶进行稳态扫描,采用稳态模式(steady state flow step)测定样品的剪切稀化特性。流变仪测试温度仍设为25 ℃,剪切速率范围从0~300 s-1,间隙设置为0.05 mm,夹具仍使用40 mm、2°的锥板。
2.7.3 淀粉糊的触变性测定 将淀粉凝胶进行稳态扫描,采用稳态模式测定样品的触变性。流变仪测试温度仍设为25 ℃,剪切速率范围从300~0 s-1,间隙设置为0.05 mm,夹具仍使用40 mm、2°的锥板。
试验数据用SPSS 16.0 for Windows 统计分析软件和Microsoft Excel 2003 数据处理系统进行统计处理。计算标准偏差(±SE)或进行差异显著分析,利用Origin 7.5 数据分析和制图软件对数据作图,各试验均重复进行3 次。
如图1所示,原木薯淀粉颗粒形状规范性较差,呈不完整的圆球形,无脐点和轮纹,颗粒大小不均,表面光滑,重结晶后的木薯淀粉颗粒形状变化剧烈,选取视野中大小介于中间的颗粒,测量得到贮存4 ℃的木薯淀粉重结晶后颗粒粒径从10 μm 增大到60 μm,颗粒结构由层状轮纹结构变为致密的纤维状结构。木薯淀粉在重结晶过程中颗粒剧烈增大,说明木薯淀粉在重结晶的过程中颗粒之间发生聚集,重结晶发生在颗粒外部。这主要是由于木薯淀粉糊化过程中,链淀粉溶出并参与重结晶,使得颗粒与颗粒发生聚集。颗粒结构由层状轮纹结构变为致密的纤维状结构。

图1 原淀粉及重结晶淀粉的扫描电子显微镜图
Fig.1 Scanning electron micrographs of native and retrogradated tapioca starch
3.2.1 结晶结构 HHP 糊化木薯淀粉贮藏在4℃及25 ℃,40 d 后进行结晶结构变化的X-衍射分析。结果发现2θ 在15.3,17.2,17.8,22.9 处出现特征吸收峰,介于A 型与B 型之间,则木薯淀粉的晶型为C 型,4 ℃结晶度数值明显高于25 ℃的结晶度值(表1),说明4 ℃重结晶程度比25 ℃大。HHP 糊化木薯在25 ℃重结晶时,其X-衍射图谱中2θ 为26°的地方有明显的增强峰(图2),该峰对应的是木薯淀粉链脂结构,则25 ℃时木薯淀粉的晶型由C 型向V 型转变,说明高温(温度为25℃)比低温(4 ℃)更容易使链脂结构重新形成。因为直链淀粉的结晶速度比支链淀粉的结晶速度快,贮存初期淀粉的重结晶主要由直链淀粉引起,后期主要由支链淀粉引起[17],判定4 ℃时更容易重结晶。
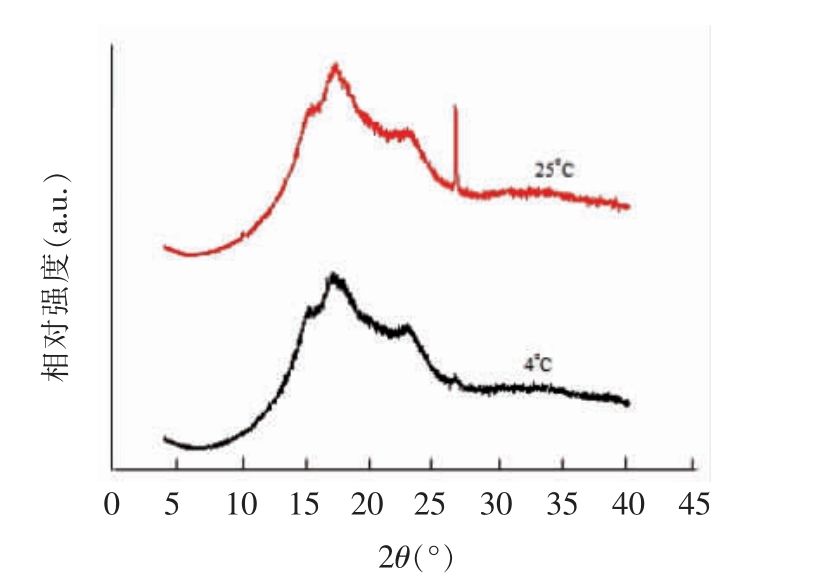
图2 木薯淀粉在不同温度下的重结晶的X-衍射图谱
Fig.2 X-ray powder diffraction patterns of retrograded tapioca starch treated at different temperature
3.2.2 水分分布 如图3所示,重结晶后淀粉中的水可分3 种类型:结合水、自由水、处于结合水和自由水之间的水[18]。0.1~1 ms 部分的水分其T2最小,因此为体系中流动性最弱的水分,即结合水。且在淀粉颗粒中结合水所占比例最大。1~30 ms 之间的峰为流动性介于结合水和自由水之间的水分。30~100 ms 之间的峰代表最大为自由水,T2 值最大。由图3可以看出,自由水、介于结合水与自由水之间的水的T2 的分布最窄,且没有规律。当淀粉颗粒中的结合水和底物紧密结合时,它就高度地固定,T2 会降低;而游离水流动性好,有较大的T2。这样,就可以得知水分结合力及结合程度[19]。木薯淀粉4 ℃的T2 值小于25 ℃的T2 值,意味着4 ℃体系中的大分子与水分子结合得更为紧密,水分子的流动性减弱,体系的弛豫速度加快,横向弛豫时间T2 减小,产品也具有更好的稳定性。
表1 木薯淀粉在不同温度下重结晶的X-衍射参数
Table 1 X-ray powder diffraction parameters of retrograded tapioca starch treated at different temperature

木薯淀粉样品结晶形式 RC/%4 ℃ C 25.54±2.50 25 ℃ C 5.53±0.49
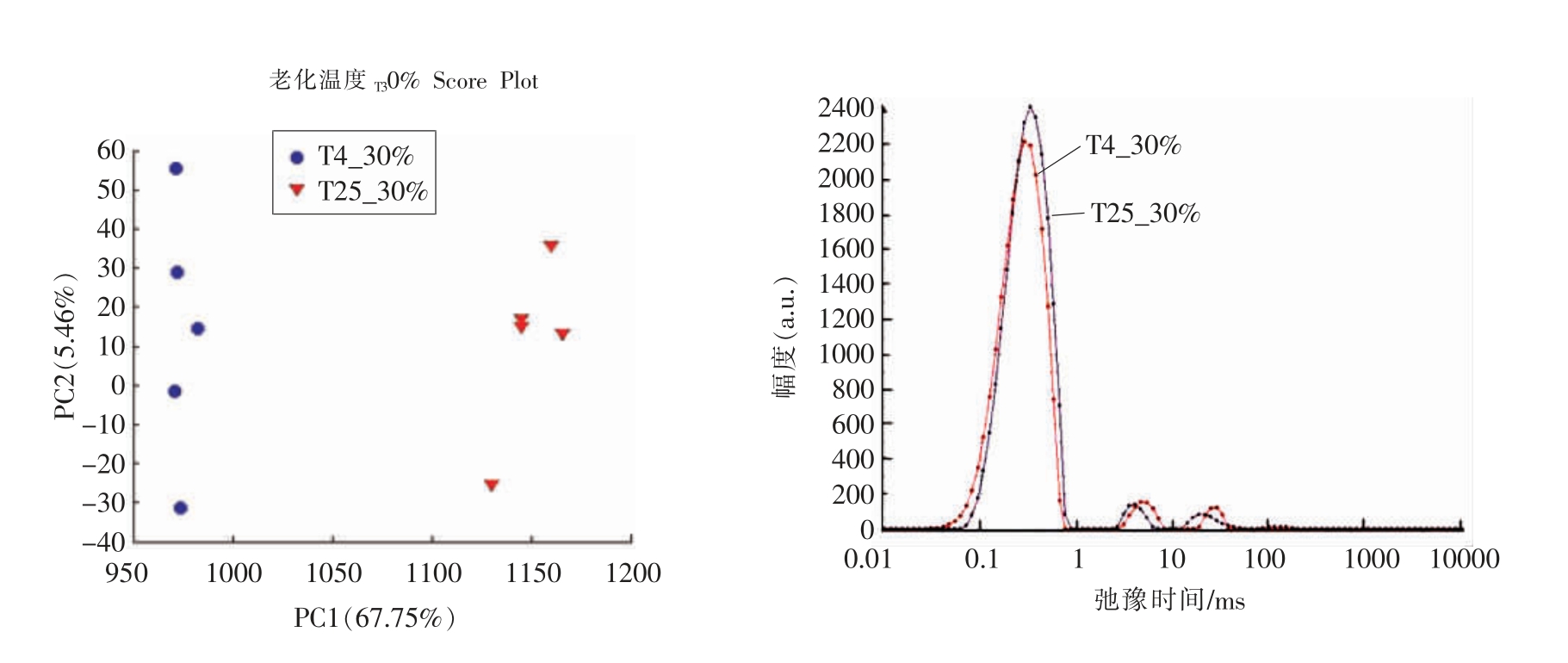
图3 木薯淀粉在不同温度下的重结晶的低场核磁共振图谱
Fig.3 Low-field NMR patterns of retrograded tapioca starch treated at different temperature
3.2.3 近程分子结构 图4为HHP 糊化木薯淀粉在4 ℃及25 ℃重结晶后的红外吸收光谱图,图中没有出现新的吸收峰或发生某个特征峰的消失,重结晶后的糊化木薯淀粉在3 100~3 700 cm-1处的吸收峰4 ℃比25 ℃的峰窄,说明重结晶后的糊化木薯淀粉在4 ℃时的分子间氢键减少,结构更加致密。从而可知4 ℃的重结晶程度比25 ℃的大,糊化的木薯淀粉在4 ℃时更容易重结晶。
FTIR 可以用来研究不同淀粉颗粒在近程分子结构水平方面的差异,对淀粉结晶,分子链构象及螺旋结构的改变十分敏感[20]。淀粉的近程结构指淀粉分子中的直链淀粉和支链淀粉中短链部分形成的双螺旋结构,而不包括双螺旋分子链通过分子间的相互作用力以一定的空间点阵在淀粉颗粒的某些区域形成不同的晶型,即远程结构[20-21];因此利用红外光谱技术也不能探究不同晶型结构(如A-型淀粉与B-型淀粉)的结构差异[22]。但可以从不同的淀粉红外光谱图的差异中得出淀粉颗粒内部有序结构部分(结晶区)和无序结构部分(无定形区)的分布比例变化情况,淀粉的红外光谱图中有3 个典型的振动吸收峰区域,对应的波数分别 在995 cm-1,1 022 cm-1 和1 045 cm-1 周 围[23]。其中波数为1 045 cm-1 周围对应的吸收峰与淀粉的结晶结构有关,对应于淀粉聚集态结构中的有序结构,可揭示短程分子内的有序结构,所对应的吸收峰的强度通常随淀粉结晶度的增加而增加,波数为1 022 cm-1 对应的吸收峰的强弱与淀粉颗粒中无定形区域原子的振动有关,因为该波数下对应的吸收峰的强度随淀粉结晶度的增加而减小。波数为995 cm-1 周围所对应的吸收峰与-C=OH 基团的弯曲振动有关,且通常其变化对淀粉的水分含量较敏感,这是因为氢键的振动与-C=OH-的振动有相似的频率,因此995 cm-1 对应的红外吸收峰强弱可用来表征淀粉结晶区域的水合程度,通常可用来表示淀粉颗粒在短程范围内的结晶程度[22]。930 cm-1 附近的吸收峰则是葡萄糖环的振动吸收峰[22,24-25]。(1 045/1 022)cm-1 和(1 022/995)cm-1 峰强度比值被看作是淀粉有序结构的指标,其中(1 045/1 022)cm 峰强度比值反映淀粉分子的有序程度,其比值越大,有序度越高[22,24-25]。
3.2.4 温度对重结晶木薯淀粉糊黏度性质的影响图5是4 ℃及25 ℃的条件下贮存3 d 的HHP糊化木薯淀粉重结晶的RVA 图。从图中可以看出,4 ℃重结晶后木薯淀粉的PV、TV、FV 都比25℃重结晶淀粉的大。这是由于4 ℃时淀粉重结晶程度较大,支淀粉有序化较强;根据曲线趋势,其崩解能力及回生性几乎没有差异。由于4 ℃重结晶程度更大,颗粒热糊化需要的PT 增加,Pt 缩短。
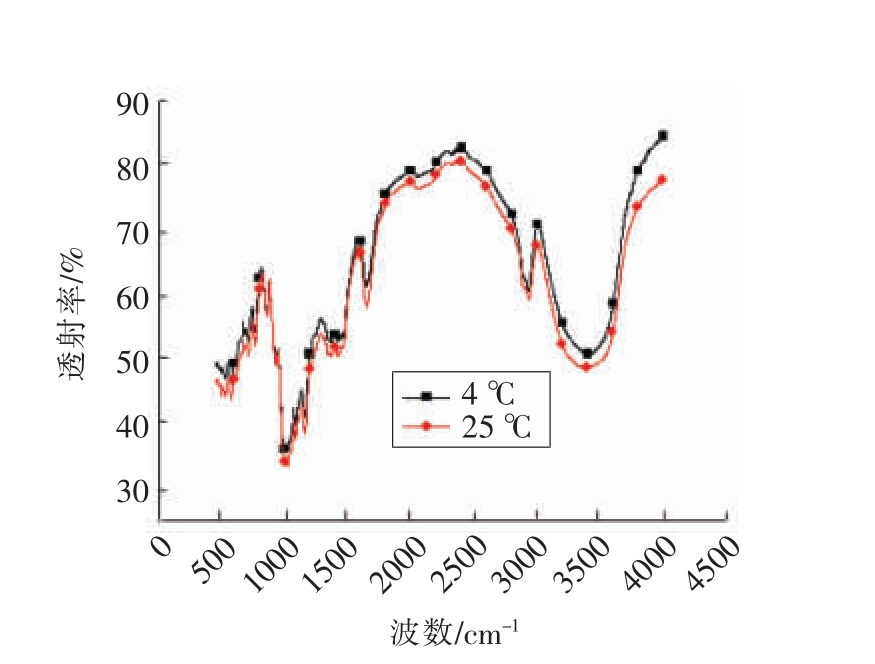
图4 不同温度贮存的高静压糊化木薯重结晶后红外吸收光谱图
Fig.4 FTIR spectra of recrystallization about HHP-induced gelatinized cassava stored at different temperatures
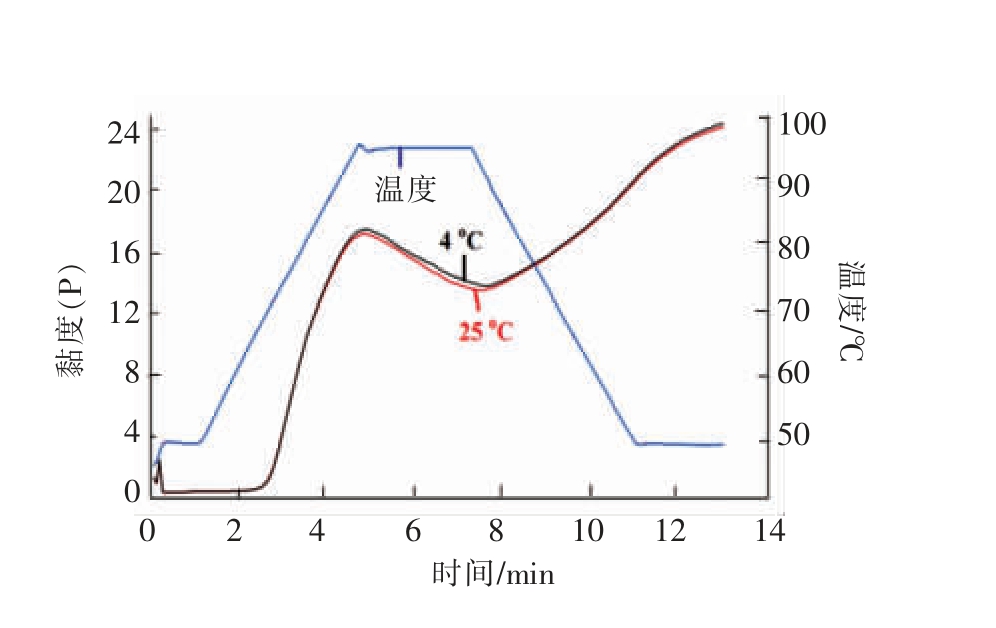
图5 不同温度贮存的高静压糊化木薯淀粉重结晶后的RVA 图
Fig.5 RVA spectra of recrystallization about HHP-induced gelatinized tapioca storing at different temperature
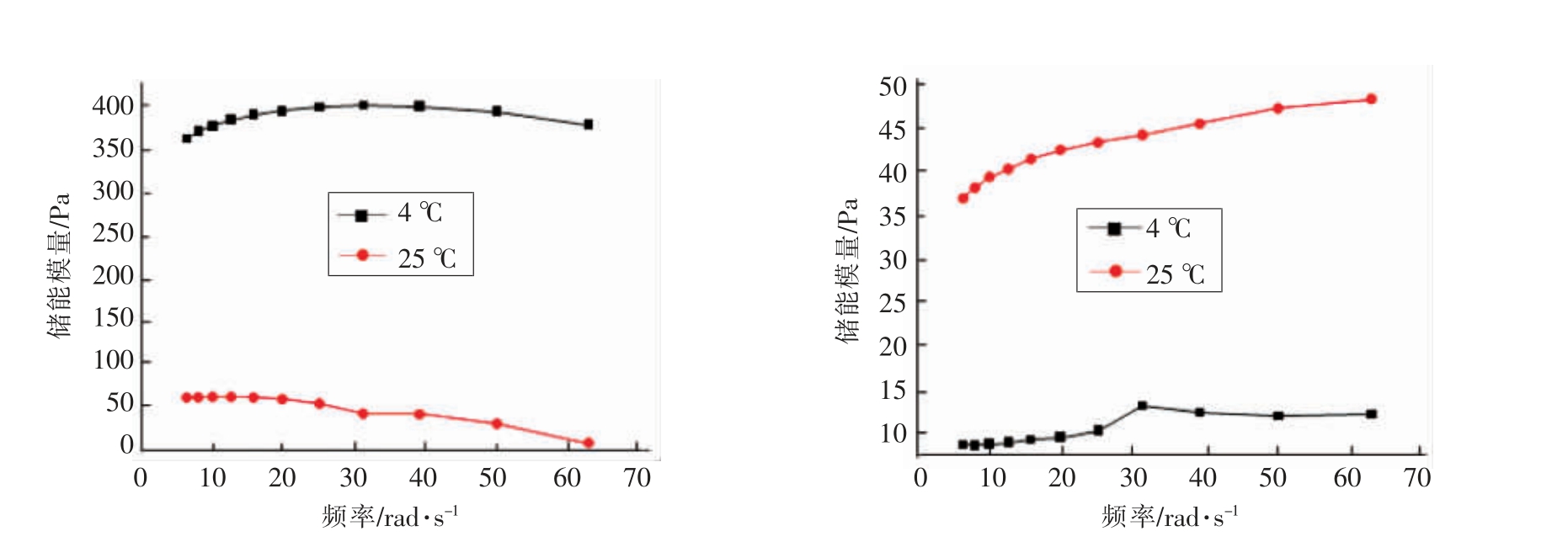
图6 不同温度木薯淀粉重结晶的流变学性质图流变学曲线
Fig.6 Pasting viscosity profiles of retrograded tapioca starch at different temperature
3.2.5 温度对重结晶木薯淀粉流变性质的影响图6是4 ℃及25 ℃的条件下贮存40 d 的木薯淀粉重结晶后的流变性质图。重结晶后,木薯淀粉的两种模量的变化曲线仍然为平滑曲线。说明HHP糊化木薯淀粉重结晶后的凝胶性弱。木薯淀粉在25 ℃和4 ℃重结晶后G′稍有下降,G′′稍有上升,且4 ℃比25 ℃的G′值大很多,G′′小很多,说明4℃重结晶的木薯淀粉具有较强的刚性特征,而凝胶性较弱。
木薯重结晶淀粉经历了加温剪切、降温、振荡测试等过程,淀粉颗粒结构在加温剪切过程中受到了最大程度的破坏,且选取的剪切速率的范围也较大(0~300 s-1),在剪切过程中淀粉由原来交织的网络结构的静态状态转变为沿流体方向作定向流动的动态状态。木薯重结晶淀粉的流变曲线均在剪切速率小于25 s-1 时出现应力低谷值,随后剪切应力随着剪切速率的增加而继续增加 (图7)。木薯重结晶淀粉都没有发现剪切稀化现象。随着剪切速率的增加,剪切压力反而逐渐增加。淀粉在流变学曲线中首先出现的应力极大是由于随着剪切速率的增大,淀粉凝胶本身强度相对较高,需要较大的应力来破坏网络结构,使越来越多的淀粉分子从凝胶结合状态转变为定性流动状态[26],几乎无链淀粉溶出,25 ℃的重结晶样品中水分子通过氢键形式结合发生的水合作用趋势较弱,因此在特定的剪切力下,淀粉凝胶强度相对比4 ℃高,且表现出剪切稀化的迹象。木薯淀粉分子的溶出相对较多。从而导致了木薯淀粉水合作用较强。且4 ℃重结晶比25 ℃重结晶的木薯淀粉凝胶强度强。
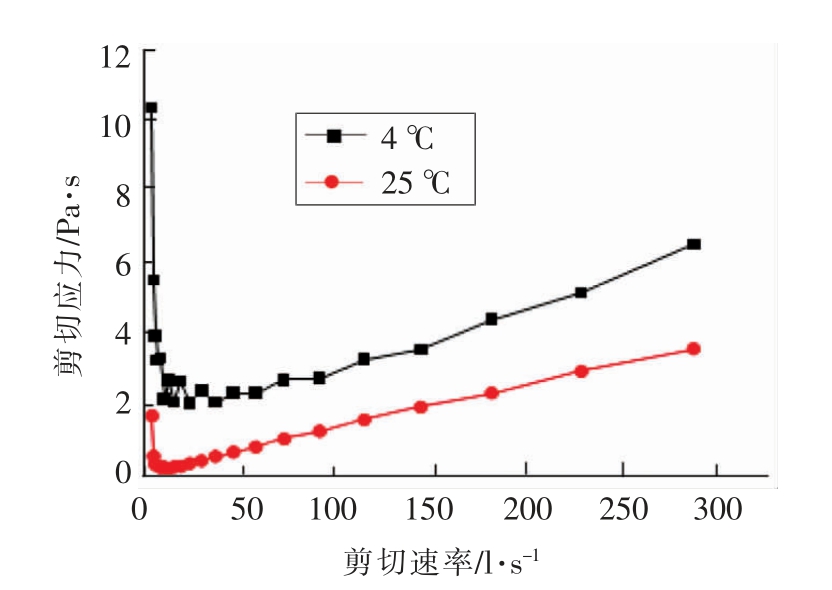
图7 不同温度木薯淀粉重结晶的剪切应力曲线
Fig.7 Sheer stress of retrograded tapioca starch at different temperature
3.3.1 结晶结构 如图8所示,在4 ℃贮藏下,随着保藏时间的延长,淀粉重结晶程度加深;低温保存2~8 d,木薯淀粉的X-衍射结果几乎没有可见的变化。早期就有学者发现马铃薯的抗老化性能较好,短期内的糊化淀粉几乎不发生老化,在DSC检测中,即使进行多次冻融循环也几乎观察不到老化现象[27]。当贮藏到40 d 时,结晶度增加到25.54。因此一方面认为木薯淀粉在短期内不发生重结晶,另一方面,木薯淀粉由于链淀粉的溶出,重结晶无法复原到原来溶出的颗粒当中,使颗粒之间发生聚集态纤维化,形成不可逆的改变,颗粒内发生塑化或者支淀粉形成缺陷结晶,X-衍射技术无法检测出。所以结合红外的短程有序结构检测。

图8 不同重结晶时间木薯淀粉的X-衍射图谱
Fig.8 X-ray powder diffraction patterns of retrograded tapioca starch treated at different starch concentration time
表2 不同重结晶时间木薯淀粉的X-衍射参数
Table 2 X-ray powder diffraction parameters of tapioca starch after different retrogradation time
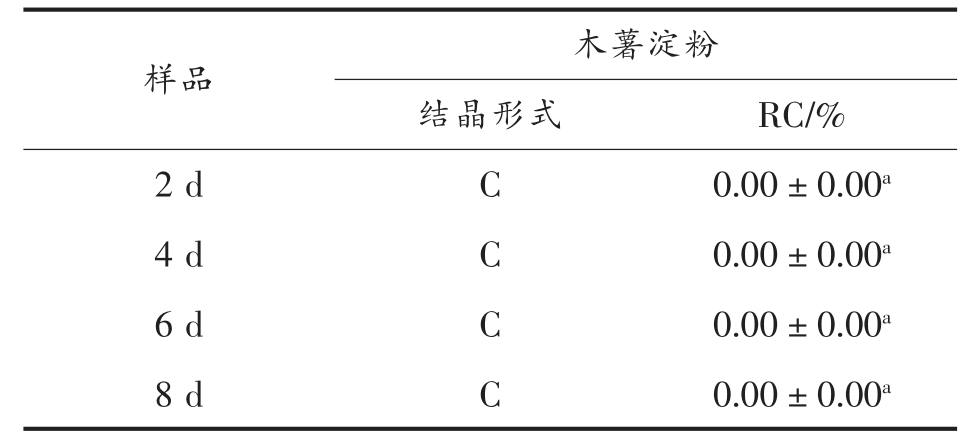
注:RC 值是3 次测定的平均值±SD;共享列中不同大写字母的值明显不同(P<0.05)。
木薯淀粉样品结晶形式 RC/%2 d C 0.00±0.00a 4 d C 0.00±0.00a 6 d C 0.00±0.00a 8 d C 0.00±0.00a
3.3.2 水分分布 如图9所示,保持50%淀粉质量分数不变,比较重结晶2 d 及8 d 样品的信号。总体上木薯淀粉老化时间PCA 分类清晰,T2 谱中主峰,8 d 重结晶后T2 时间稍长于2 d 重结晶后的样品。自由水、介于结合水与自由水之间的水的T2的分布最窄,且没有规律。结合水所占比例最大。当淀粉颗粒中的结合水和底物紧密结合时,其高度固定,T2 会降低;而游离水流动性好,有较大的T2。这样,就可以得知水分结合的力和程度[23]。木薯淀粉2 d 的T2 值小于8 d 的T2 值,意味着重结晶2 d 后体系中的大分子与水分子结合得更为紧密,水分子的流动性减弱,体系的弛豫速度加快,横向弛豫时间T2 减小,产品也具有更好的稳定性[28]。随着重结晶时间的延长,结合水的结合能力逐渐降低,对应的T2 延长,水的移动性增加。其原因可能是重结晶过程,支链淀粉倾向有序排列,水分被挤出结晶区,这部分水的弛豫时间介于自由水和不可移动水之间。
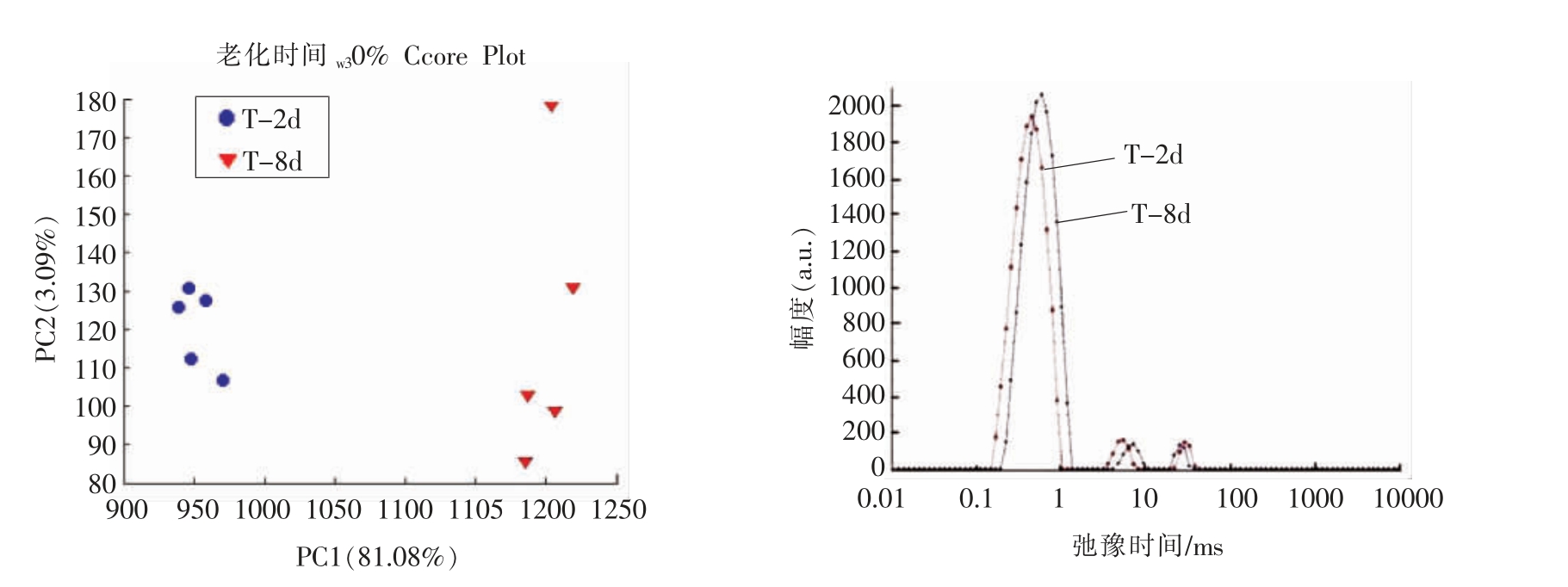
图9 不同重结晶时间木薯淀粉的低场核磁共振图谱
Fig.9 Low-field NMR patterns of retrograded tapioca starch treated at different time
3.3.3 近程分子结构 图10为HHP 糊化木薯淀粉重结晶后的红外吸收光谱图,由图可知在3 100~3 700 cm-1 范围内,较宽的吸收峰是淀粉分子链中分子间或分子内自由羟基(-OH)的伸缩振动吸收峰;1 154.24 cm-1 为与伯、仲醇羟基相连的C-O 键和吡喃糖环的C-O 键的伸缩振动吸收峰,929.57,861.14,765.24 和709.72 cm-1 处是葡萄糖环的特征性吸收峰,其中927 cm-1 处为D-吡喃葡萄糖的非对称伸缩振动峰;576.63,5 765.24 和861.14 cm-1 处是-CH2 的摇摆振动吸收特征峰[29-31],这与无定形结构及更为有序结构的形成有关。通过对不同压力条件下红外吸收光谱图的比较,木薯淀粉在重结晶6 d 及8 d 后特征峰几乎消失,说明淀粉分子间或分子内相互通过氢键作用连接排列的作用方式被扰乱,自由羟基通过其他方式形成了更为精密的连接方式,颗粒内部发生塑化或重新有序化为缺陷结晶,形成正如扫描电镜中聚合态纤维化的木薯淀粉。
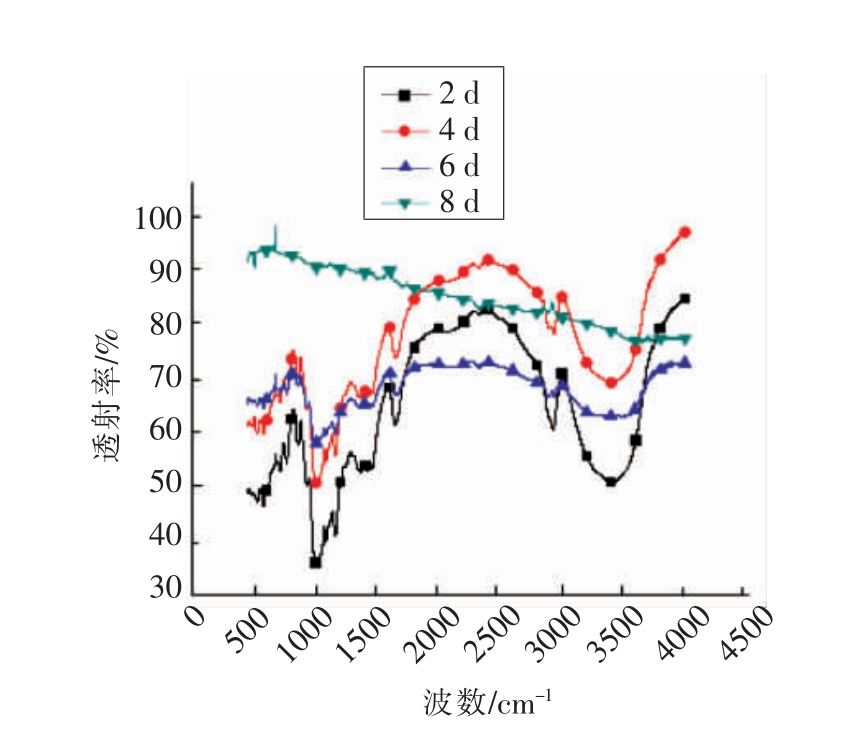
图10 不同时间贮存的高静压糊化木薯重结晶后红外吸收光谱图
Fig.10 FTIR spectra of recrystallization about HHP-induced gelatinized tapioca after different storing time
3.3.4 时间对重结晶木薯淀粉流变性质的影响图11为4 ℃条件下贮存2,4,6,8 d 的HHP 糊化糯玉米及木薯淀粉重结晶后的流变性质图,重结晶后木薯原淀粉仍然为平滑曲线,说明HHP 糊化木薯淀粉重结晶后仍然表现为弱凝胶。随着时间的延长,G′及G′′值都增大。该结果表明,随着重结晶时间的延长,木薯淀粉的刚性增加,凝胶性也增加,重结晶8 d 后,曲线出现交叉现象,木薯淀粉从典型的弱凝胶体系转变为强凝胶。
如图12所示,随着重结晶时间的延长,木薯淀粉发生剪切稀化现象,糯木薯淀粉剪切应力在2,4,6 d 时,剪切应力为0,也几乎不随剪切速率的增大而增大,当重结晶时间达到8 d 时,才显示出凝胶性,有一定的剪切应力,但是随着剪切速率的减小而减小,表现出剪切稀化迹象。
1)木薯淀粉在重结晶过程中颗粒发生聚集,重结晶发生在颗粒外部。
2)温度对重结晶的影响:4 ℃重结晶程度比25 ℃大;木薯淀粉在短期内不发生重结晶。4 ℃重结晶后木薯淀粉的PV、TV、FV 都比25 ℃重结晶淀粉的大。
3)时间对重结晶的影响:HHP 糊化木薯淀粉重结晶后的凝胶性弱。随着重结晶时间的延长,木薯淀粉的刚性增加,凝胶性也增加,重结晶8 d后,曲线出现交叉现象,木薯淀粉从典型的弱凝胶体系转变为强凝胶。随着重结晶时间的延长,木薯淀粉发生剪切稀化现象,剪切应力在2,4,6 d 时,剪切应力都为0,当重结晶时间达到8 d 时,才显示出凝胶性,有一定的剪切应力,但是随着剪切速率的减小而减小,表现出剪切稀化迹象。
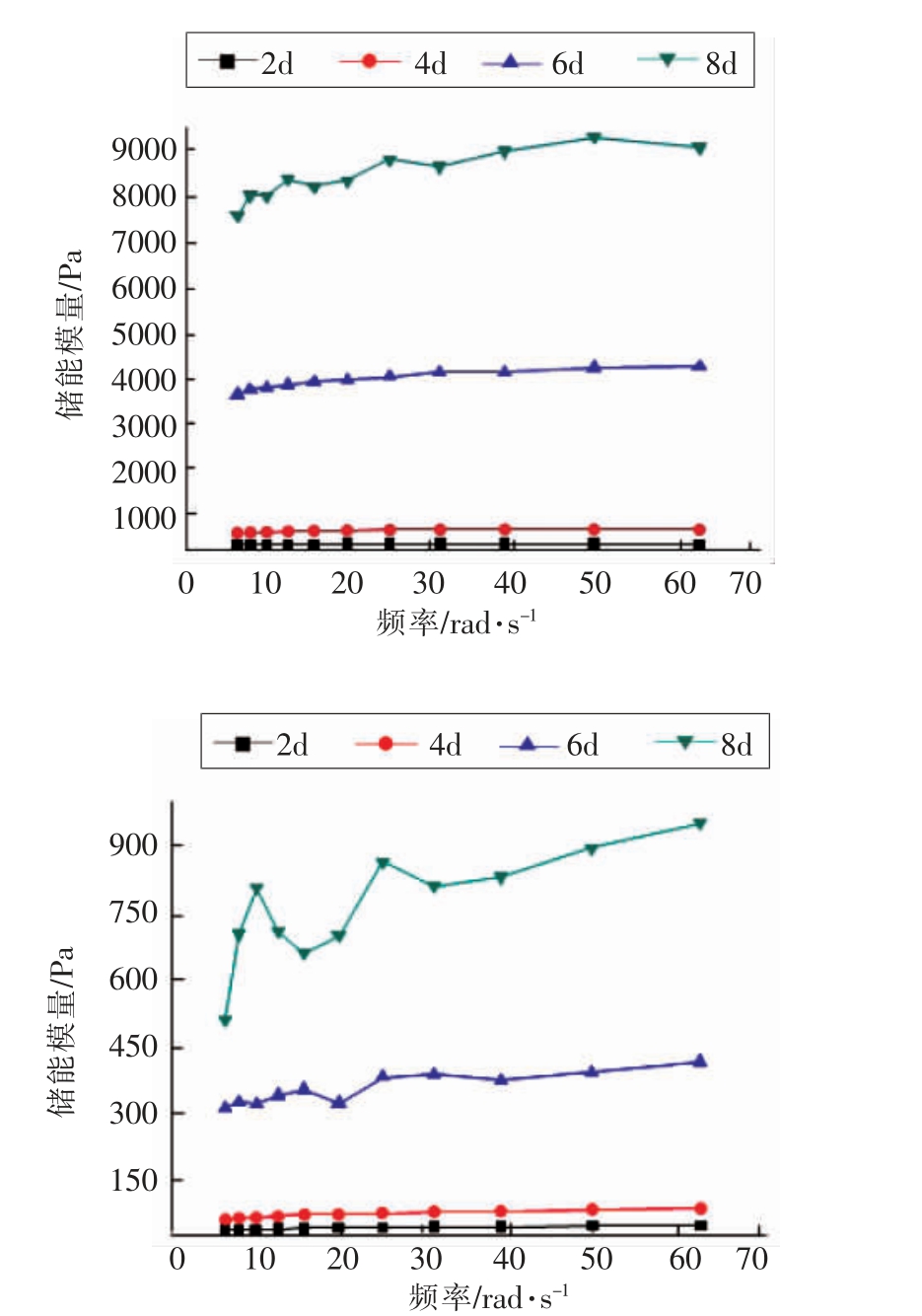
图11 不同重结晶时间木薯淀粉的剪切力曲线
Fig.11 Shear force curve of tapioca starch after different retrogradation time
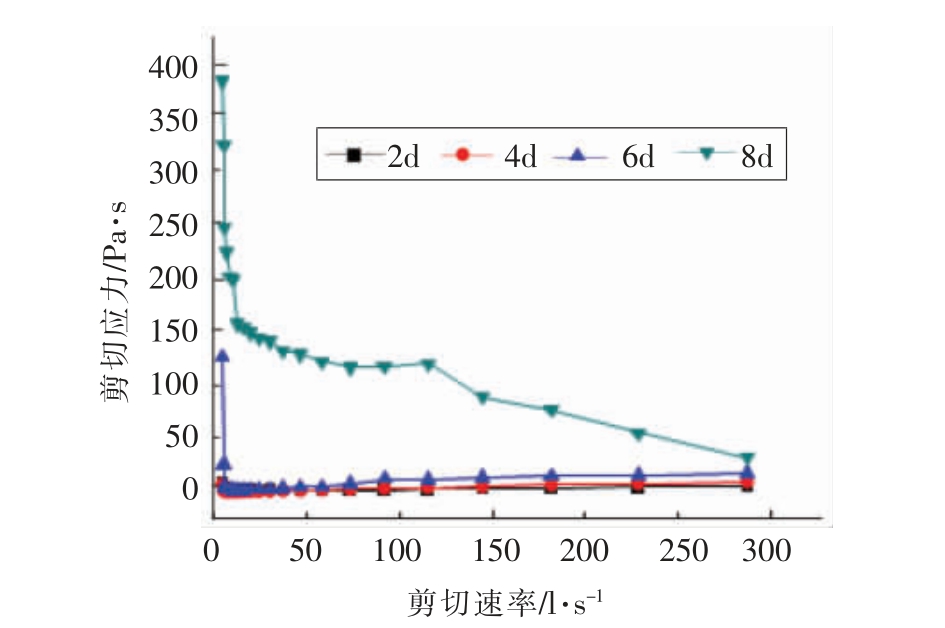
图12 不同重结晶时间木薯淀粉的流变性质图
Fig.12 Rheological properties of tapioca starch after different retrogradation time
[1]FARR D.High pressure technology in the food industry[J].Trends Food Sci Tech,1990,1(90):14-17.
[2]MERTENS B,KNORR D.Development of nonthermal processes for food preservation[J].Food Technol,1992,46(5):124-133.
[3]CAMERON R E,DONALD A M.A SAXS study of the absorption of water into the starch granule[J].Carbohydrate Research,1993,244(2):225-236.
[4]ELIASSON A C.starch in food:Structure,function and applications[M].New York:CRC Press,2004.
[5]WAIGH T A,GIDLEY M J,LOMANSHEK B U,et al.The phase transformations in starch during gelatinization:a liquid crystalline approach[J].Carbohydrate Research,2000,328(2):328.
[6]WAIGH T A.KATO K L,DONALD A M,et al.Side-chain -liquid -crystalline model for starch [J].Starch/Starke,2000,52(12):450-460.
[7]丁文平.大米淀粉回生及鲜湿米线生产的研究[D].无锡:江南大学,2003.
[8]DOUZALS J P,CORNET J M P,GERVAIS P,et al.High-pressure gelatinization of wheat starch and properties of pressure-induced gels[J].Journal of Agriculture of Food Chemistry,1998,46(12):4824-4829.
[9]KING A,KALETUNÇ G.Retrogradation characteristics of high hydrostatic pressure processed corn and wheat starch[J].Journal of Thermal Analysis and Calorimetry,2009,98(1):83-89.
[10]HU X T,XU X M,JIN Z Y,et al.Retrogradation properties of rice starch gelatinized by heat and high hydrostatic pressure (HHP)[J].Journal of Food Engineering,2011,106(3):262-266.
[11]周海宇.高静压酯化木薯淀粉结构及其理化性质的研究[J].现代食品科技,2016,32(2):107-112.
[12]黄峻榕.X-射线衍射在测定淀粉颗粒结构中的应用[J].陕西科技大学学报,2003,21(4):90-93.
[13]LORENZ K,KULP K.Steeping of wheat starches at various temperatrues.Effects on physicochemical characteristics of the starch[J].Starch/Stärke,1978,30(10):333-336.
[14]左春柽,张守勤.高压处理玉米淀粉的X-射线衍射图谱分析[J].农业工程学报,1997,13 (2):206-210.
[15]张本山,杨连生.玉米预糊化淀粉结晶性质的研究[J].华南理工大学学报(自然科学版),1997,25(2):107-111.
[16]CHEN F L,WEI Y M,ZHANG B.Characterization of water state and distribution in textured soybean protein using DSC and NMR[J].Journal of Food Engineering,2010,100(3):522-526.
[17]王婷婷,冯霞,连喜军.淀粉回生动力学研究进展[J].食品加工,2016,41(1):39-43.
[18]HANASHIRO I,ITOH K,KURATOMI Y,et al.Granule-bound starch synthase I is responsible for biosynthesis of extra-long unit chains of amylopectin in rice[J].Plant and Cell Physiology,2008,49(6):925.
[19]ZIMERI J,KOKINI J.Rheological properties of inulin-waxy maize starch systems[J].Carbohydrate Polymers,2003,52(1):67-85.
[20]GALLANT D J,BOUCHET B,BALDWIN P M.Microscopy of starch:evidence of a new level of granule organization[J].Carbohydr Polym,1997,32(3/4):177-191.
[21]CHEETHAM N W H,TAO L.Variation in crystalline type with amylose content in maize starch granules:an X-ray powder diffraction study[J].Carbohydr Polym,1998,36(4):277-284.
[22]SEVENOU O,HILL S E,FARHAT I A.Organisation of the external region of the starch granule as determined by infrared spectroscopy[J].International Journal of Biological Macromolecules,2002,31(1/2/3):79-85.
[23]VARATHARAJAN V,HOOVER R,LIU Q,et al.The impact of heat-moisture treatment on the molecular structure and physicochemical properties of normal and waxy potato starches [J].Carbohydrate Polymers,2010,81(2):466-475.
[24]SHINGEL K I.Determination of structural peculiarities of dexran,pullulan and -irradiated pullulan by Fourier-transform IR spectroscopy[J].Carbohydr Res,2002,337(16):1445-1451.
[25]SMITS A L M,RUHNAU F C,WLIEGENTHART J F G,et al.Ageing of starch based systems as observed with FT-IR and solid state NMR spectroscopy[J].Starch,1998,50(11/12):478-483.
[26]HOPKINS S,GORMLEY R.Rheological properties of pastes and gels made from starch separated from different potato cultivars[J].Lebensmittel-Wissenschaft und-Technologie,2000,33(5):388-396.
[27]HAN M,ZHANG Y,FEI Y,et al.Effect of microbial transglutaminase on NMR relaxometry and microstructure of pork myofibrillar protein gel[J].European Food Research and Technology,2008,228(4):665-670.
[28]CAEL J J,KONEIG J L,BLACKWELL J.Infrared and Raman Spectroscopy of carbohydrates.Part VI:Normal coordinate analysis of V-amylose[J].Biopolymers,1975,14(9):1885-1903.
[29]SEVEBO O,HILL S E,FARHAT I A,et al.Organisation of the external region of the starch granule as determined by infrared spectroscopy[J].Int J Bio Macromol,2002,31(1):79-85.
[30]CAPRON I,ROBERT P,COLONNA P,et al.Starch in rubbery and glassy states by FTIR spectroscpy[J].Carbohyd Polym,2007,68(2):249-259.
[31]ZIMERI J,KOKINI J.Rheological properties of inulin-waxy maize starch systems[J].Carbohydrate Polymers,2003,52(1):67-85.
Recrystallization Properties of High Hydrostatic Pressure Induced Gelatinized Tapioca Starch