冻藏和解冻是牛肉加工、贮藏、运输中的重要环节。使用不当的解冻方法,直接影响牛肉产品的色泽、风味、质地等重要食用指标,造成汁液流失与品质劣变。目前,肉类的解冻技术主要包括空气解冻[1]、水解冻[2]、冰箱解冻[3-4]、微波解冻[5]、超声波解冻技术和超高压解冻[6]等。每种解冻技术既各具优点,又存在一些不足。例如,自然解冻时间长,容易造成品质下降;水解冻容易造成色泽、风味和质量差;冰箱解冻效率低,汁液损失大;微波解冻容易造成物料不均匀;超高压解冻设备价格昂贵,能耗较高。鉴于此,探索新的牛肉解冻技术势在必行。
高压电场解冻技术是一种新型非热食品解冻技术,具有解冻速度快,解冻品质优,操作简单,抑制微生物等优点[7-8],正在成为一个研究热点。Rahbari 等[9]在多针-板电极系统中进行冷冻鸡胸肉的解冻试验,发现3 kV/cm 条件下的解冻时间比对照组降低2.3 倍。Li 等[10]在电压12 kV 时对鲤鱼进行解冻,发现汁液流失率比对照组低2.95%,初始细菌总存活数、气单胞菌、假单胞菌和乳酸菌分别下降0.47,0.22,0.17,0.34 lg CFU/g。He 等[11]用高压电场解冻猪肉,5 d 后猪肉挥发性碱性氮(VBN) 值从10.64 mg/100 g 增至16.38 mg/100 g,而对照组猪肉VBN 值从10.66 mg/100 g 增至19.87 mg/100 g,表明高压电场解冻可以延长猪肉的保质期。高压电场解冻的能耗远低于微波解冻,且解冻时间、电压和能耗之间分别满足二次函数关系[12]。Mousakhanian-ganjeh 等[13-14]发现在高压电场作用下,金枪鱼的解冻速率是对照组的1.78倍,并且很好地保持了产品质量,解冻速度和能耗随电压的升高和极距的降低而升高。Amiri 等[15]在高压电场作用下进行牛肉解冻试验,结果表明针电极数量增加牛肉解冻损失率、蒸发损失率、蒸煮损失率和总损失率降低,持水性、溶解度和肌原纤维蛋白的凝胶强度先降低后升高。
近年来,红外光谱技术因无损,不使用化学试剂,操作简单,样品用量少和重复性好等优点而受到研究者的青睐,成为一种重要的分析手段[16-17]。Zhuang 等[18]利用近红外和远红外光谱法鉴别出4个地区的山药样品,并分析了山药样品的总糖、多糖和黄酮类化合物。Acri 等[19]通过分析不同地区、不同品种大蒜的红外光谱吸收峰的差异,对食品进行了分类。这些研究均表明红外光谱技术在对物料成分的鉴别方面效果非常好,然而,至今尚未发现关于对高压电场解冻,用牛肉红外光谱分析,特别是共有峰率和变异峰率的双指标序列方面的详细报道。
本文研究多针-板电极系统中不同针间距对牛肉解冻特性的影响,测定解冻过程中牛肉的解冻特性和品质参数,分析蛋白质的二级结构以及共有峰率和变异峰率的双指标序列,旨在为高压电场解冻技术在牛肉解冻中的应用提供试验依据,也为红外光谱拓展到高压电场解冻领域提供技术支撑。
1 材料与方法
1.1 仪器及设备
高压电场解冻装置(见图1)由高压电源(YD(JZ)-1.5 / 50,武汉高压电器厂)、电压控制器(KZX-1.5KVA,武汉高压电器厂)和多针-板电极系统组成[20];BS124S 电子天平,赛多利斯科学仪器有限公司;HH-4 恒温水浴锅,荣华仪器制造有限公司;TDZ4-WS 离心机,湘仪离心机仪器有限公司;3nh-NR60CP 全自动色差计,深圳市五苏产业发展有限公司;HY-12 压片机,英国Specac 公司;Nicolet iS10 傅立叶变换红外光谱仪,日本Shimadzu 公司。
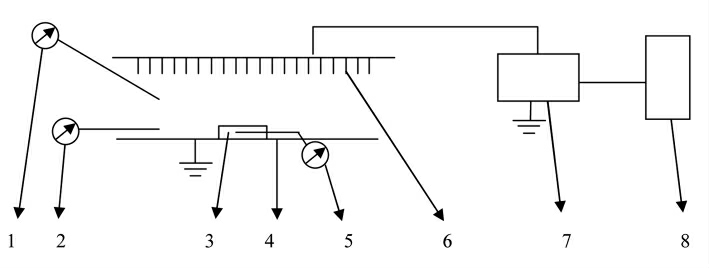
图1 高压电场解冻设备
Fig.1 High voltage electric field thawing equipment
注:1.温度计;2.湿度计;3.冷冻牛肉;4.下极板;5.温度传感器;6.多针电极;7.高压电源;8.电压控制箱。
高压电源通过电压控制器,可以输出0~50 kV 的交流高电压。交流电压的频率为50 Hz。针状电极连接到高压电源。每个针的长度和直径分别为60 mm 和1 mm。相邻针之间的距离可以调节,调节范围为2~12 cm。接地电极是100 cm×45 cm的钢板。针尖与接地电极之间的距离为10 cm。用温度计和湿度计来测量解冻过程中相应的温度和相对湿度。
1.2 试验方法
试验所用的牛肉从内蒙古呼和浩特市内蒙古工业大学附近华联超市购买。将购买的牛肉加工成3.5 cm×3.5 cm×3.5 cm 的立方体,平均质量约40 g,并立即放在-20 ℃的冰箱中冷冻24 h 后进行解冻试验。在温度为(23±1)℃,相对湿度为30%±1%,环境风速为0 m/s 条件下进行牛肉解冻试验。在多针-板电极系统中,解冻过程中电极距离和电压分别为10 cm 和28 kV。针间距分别为2,4,6,8,10,12 cm。电压为0 kV,其它试验条件与高压电场解冻条件相同的解冻试验作为对照组。解冻前,用电子天平称量冷冻牛肉块的质量,然后将温度传感器插入冷冻牛肉的几何中心。用数字温度计测量解冻过程中牛肉中心的温度。在冻牛肉块的几何中心温度为-10 ℃时开始记录。每隔5 min 记录一次温度。到牛肉样品几何中心的温度达到0℃时停止解冻试验。冷冻牛肉的中心温度从-10℃升高到0 ℃所需的时间定义为解冻时间。用电子天平测量解冻后牛肉和汁液的总质量。所有试验数据均平行独立重复测量3 次,结果采用“平均值±标准差”来表示。
1.3 测定指标
1.3.1 解冻速率 解冻过程中牛肉的解冻率定义为:
式中,m1——冷冻牛肉的质量,g;t——解冻时间,min。
1.3.2 蒸发损失率 解冻过程中牛肉的蒸发损失定义为[13]:
式中,m2——解冻后牛肉与汁液的总质量(g)。
1.3.3 汁液流失率 解冻过程中牛肉的滴水损失定义为[21]:
式中,m3——解冻后牛肉的质量(g)。
1.3.4 蒸煮损失率 根据蒸煮过程前、后牛肉样品质量的差异计算蒸煮损失[22]。将解冻的牛肉放入95 ℃的恒温水浴锅中30 min。解冻过程中牛肉的烹饪损失定义为:
式中,mx——蒸煮之前牛肉的质量(g);my——蒸煮之后牛肉的质量(g)。
1.3.5 离心损失率 根据离心过程前、后牛肉重量的差异计算离心损失[23]。将一小部分解冻的牛肉放入离心机中,以4 000 r/min 的速度离心30 min。解冻过程中牛肉的离心损失定义为:
式中,mb——离心之前牛肉的质量(g);ma——离心之后牛肉的质量(g)。
1.3.6 颜色 将解冻后的牛肉用色差计直接测其表面的亮度值L*,红度值a*,黄度值b*。先将仪器进行校正,检测时,对同一样品取5 个点,结果取平均值。
1.3.7 傅里叶变换红外光谱 将解冻的牛肉产品粉碎,并与溴化钾混合。将其置于压片机中形成半透明片状样品。用傅立叶变换红外光谱仪扫描样品,以除去水和二氧化碳的干扰,从而获得扫描光谱。用数据处理软件对获取的红外光谱进行基线校正,然后用相关图谱软件处理红外光谱原始数据。
1.3.8 红外指纹图谱共有峰率和变异峰率的测定 根据红外光谱进行红外指纹图谱共有峰率和变异峰率双指标序列分析[24],具体为:
1) 共有峰的确定方法 对于一组吸收峰,若组内吸收峰的波数最大差异显著小于其与相邻组之间的平均波数差,就确定该组峰是一组共有峰。
2) 共有峰率的定义

式中,P——共有峰率 (%);Ng——在比较的两个IR 图中都出现的吸收峰的个数;Nd——相互比较的两个IR 图中的独立峰总数;na——指纹图谱a 中相对与其共有峰的非共有峰数,称为a 的变异数;nb——指纹图谱b 中相对与其共有峰的非共有峰数,称为b 的变异数。
3) 变异峰率的定义

式中,Pva——指纹图谱a 的变异峰率 (%);Pvb——指纹图谱b 的变异峰率 (%);Na——指纹图谱a 的总峰数;Nb——指纹图谱b 的总峰数。
4) 双指标序列定义 以指纹图谱共有峰率和变异峰率的计算公式及各样品为参考,分别计算其它样品红外指纹图谱的共有峰率和变异峰率,并且根据共有峰率的大小排成一个序列(包含共有峰率和变异峰率值),该序列称为共有峰率和变异峰率双指标序列。通过该序列可以精确知道不同针间距和对照组之间的差异。
1.3.9 蛋白质二级结构测定 采用红外光谱中酰胺I 带(1 600~1 700 cm-1)的数据,通过模拟计算得到α-螺旋、β-折叠、β-转角、β-反平行和无规则卷曲对蛋白质二级结构组成的百分比[25]。
1.4 统计分析
利用单因素方差分析和显著性分析来计算高压电场和对照组条件下冷冻牛肉之间的解冻时间、解冻速率、蒸发损失率、汁液流失率、蒸煮损失率和离心损失率。当P<0.05 时为具有差异显著性。
2 结果与分析
2.1 牛肉的中心温度、解冻时间和解冻速率的测量结果
不同针间距下牛肉解冻时的中心温度曲线图,解冻时间和解冻速率的结果见图2。从图2a可以看出,在所有试验条件下牛肉的中心温度从-10 ℃到-5 ℃阶段内上升较快;从-5 ℃到0 ℃阶段内上升较慢,且各处理组之间有一定差异。还可以看出解冻过程中高压电场对从-5 ℃到0℃阶段有非常大的影响。Li 等[10]使用不同解冻方法解冻鱼肉时,发现解冻过程中鱼肉的几何中心温度在最初的几分钟内升高较快,从-5 ℃到0 ℃阶段内缓慢上升。在食品冷冻行业中,通常认为物料中心温度从-5 ℃到-1 ℃阶段内是最大冰晶形成的区域,解冻所用时间最长[11,26]。这些研究成果与本试验结果一致。
从图2b 可以看出,在高压电场下样品的解冻时间比对照组短,解冻速度快,随着针间距的变化,解冻时间和速率也发生变化。高压电场作用,不同针间距牛肉下的解冻时间从36.6 min 到50 min,分别比对照组缩短2.25 倍到3.1 倍。针间距为2,4,6,8,10,12 cm 时,解冻时间比对照组分别缩短了2.25,2.33,2.6,3.1,2.58,2.350 倍;解冻速率加快了2.23,2.23,2.54,2.96,2.48,2.29 倍。从试验结果可以看出,针间距为8 cm 时解冻效果最好。
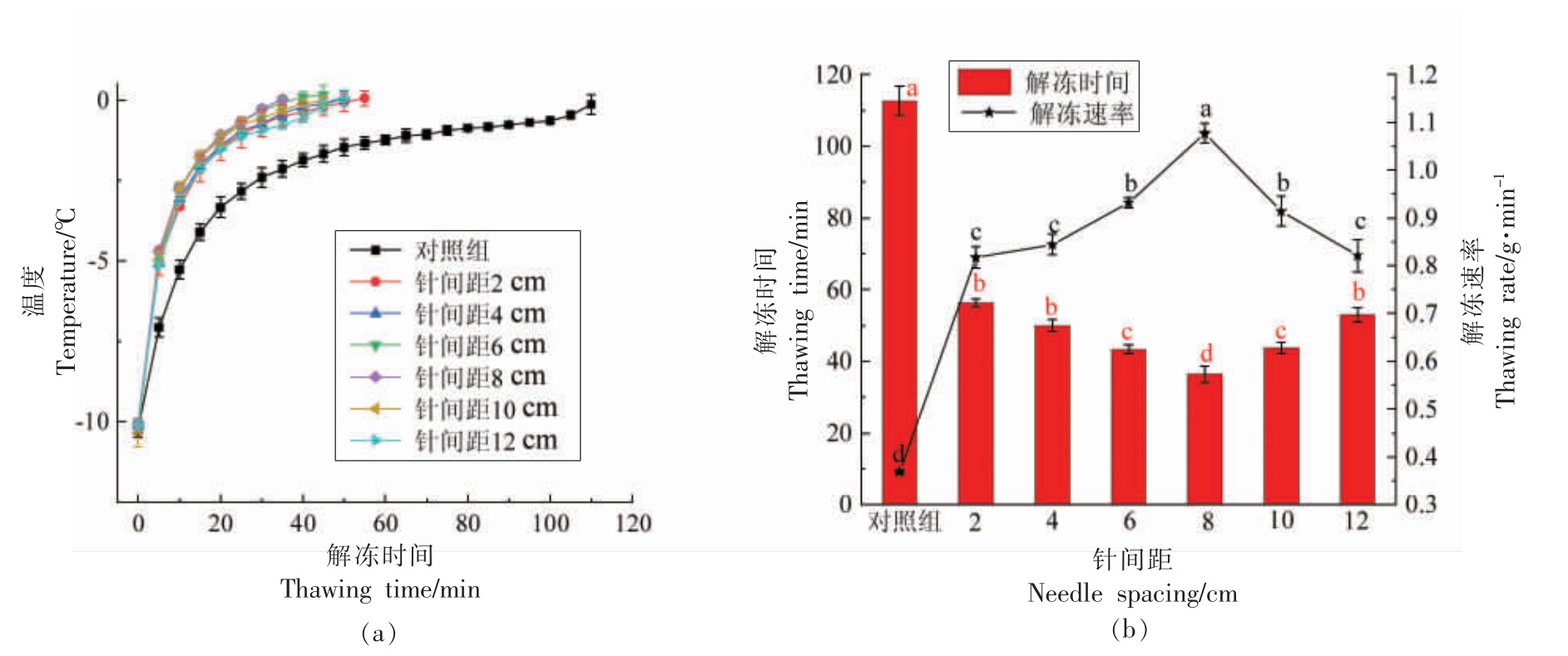
图2 针间距对解冻参数的影响
Fig.2 Effects of needle spacing on thawing parameters
注:数据显示为“平均值±标准差”,字母代表均值显著性不同(P<0.05)。
在多针-板电极系统中,高压电场作用下会使针状电极附近的空气电离成离子,在非均匀电场的作用下将产生的离子被加速,形成离子风。可以估算离子风速度的公式为[7]:
式中,ΔU——两极板之间的电压(V);d——极距(cm);ρ——空气密度(g/cm3)。
对于单针-板电极,离子分布可以用公式(13)计算[27]:
式中,j(0)——最大电流密度(A/cm2);m——方程的指数;θ=arctan(r/d);r——平面电极上距垂直中心轴的径向距离(cm);d——放电电极和接地电极之间的间隙(cm)。
外加电压与放电电流之间的关系为[27]:
式中,U——施加电压 (V);U0——电晕放电的初始电压 (V);A——接地电极面积(cm2);b——离子迁移率 (%);d——放电电极和接地电极之间的间隙(cm);g0——无量纲几何因子。
对于多针-板电极,离子分布是多个单针-板电极的叠加。图3为不同针间距下离子的电流密度分布。从图3可以看出,离子风与针间距、电压和电极距离有关。离子风的平均风速受到针间距的变化而产生影响,进而引起离子风的叠加效果发生变化。随着针间距的减小,针尖放电增强,空气中的离子数量增加,风速和风量增加。通过以上研究,发现在高压电场下,离子风对牛肉解冻速度的影响较大。因此,牛肉的解冻特性也与针间距、电压和电极距离有关。从图3b 可以看出,当电压为28 kV 时,电极距离为10 cm,针距为8 cm,解冻速度最快。在离子风的作用下,离子风与物料表面发生碰撞,并在表面上形成的边界层上引起湍流,最终导致传热系数提高,提高解冻效果。许多研究人员发现,高压电场解冻的机理主要是离子风的作用[9,15],这与本试验结果一致。
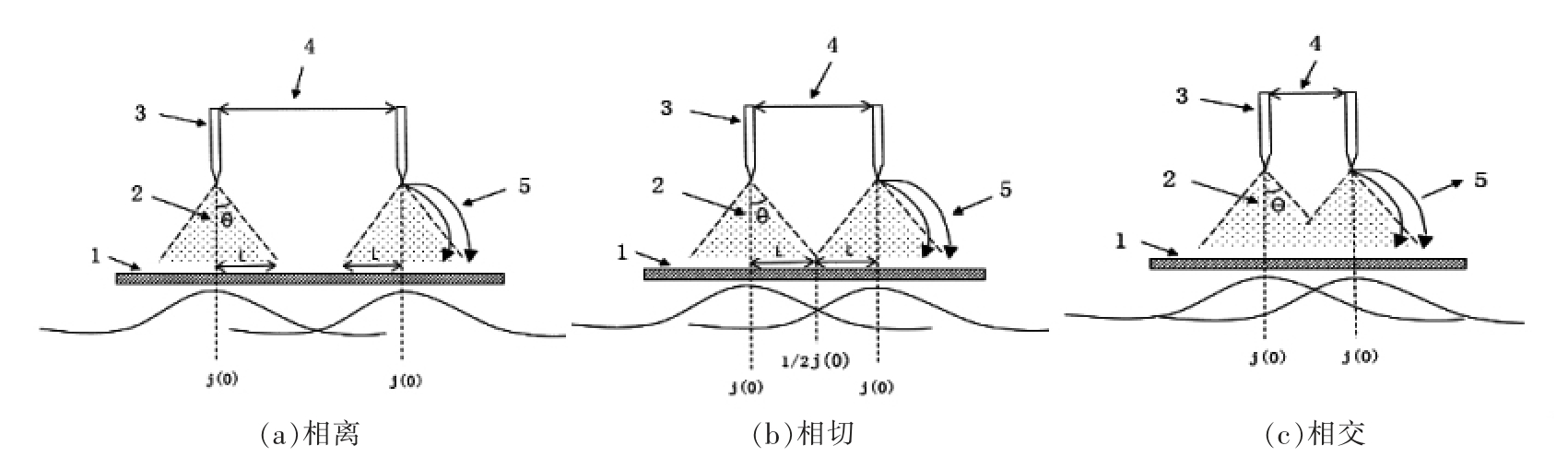
图3 离子的电流密度分布
Fig.3 Current density distribution of ions
注:1.下极板;2.极距;3.发射电极;4.相邻针电极距离;5.电场和离子流线。
2.2 汁液流失率、蒸发损失率、蒸煮损失率和离心损失率的测量结果
肌肉中的大部分水分存在于肌原纤维内,肌原纤维与肌膜之间或细胞与肌肉束之间。许多因素会影响肌肉组织中的水分流失,例如:肉的原始形式,三磷酸腺苷的流失,pH 值的降低,离子浓度变化,后期的蛋白质水解和肌原纤维收缩引起的空间效应,这都会影响持水能力[28]。如今,可以使用不同的指标来评估肉类的持水能力,包括汁液流失率、蒸发损失率、蒸煮损失率和离心损失率[29]。
表1显示了在不同解冻条件下牛肉的汁液流失率、蒸发损失率、蒸煮损失率和离心损失率的结果。消费者主要是通过牛肉大理石花纹、颜色和汁液流失率来判断肉的品质[30]。汁液流失率是在解冻过程中牛肉内部冰晶融化成水以及蛋白质组成的液体从牛肉中排出所导致的。从表1可以看出,高压电场解冻过程中牛肉的汁液流失率显著低于对照组(P<0.05)。这表明高压电场解冻可以有效减少汁液流失率。当针间距小于10 cm 时,汁液流失率没有显著差异。随着针间距的不断增加,汁液流失率也会增加。从图2可以看出,当针距大于8 cm 时,解冻时间分别为46.7 min 和53 min。如果解冻时间太长,牛肉自身的质量会使肌原纤维之间的水分流失,进而导致汁液流失率增加。牛肉在高压电场下的蒸发损失率明显高于对照组 (P<0.05)。随着针间距的增加,蒸发损失率减少。导致蒸发损失率增加的主要原因是高压电场下离子风的产生。Mousakhani-Ganjeh 等[13]解冻金枪鱼发现蒸发损失随着电压的升高而增加,这与本试验结果一致。高压电场下牛肉的蒸煮损失率显著低于对照组(P<0.05)。Hsieh 等[31]发现高压电场可以有效减少鸡大腿肉的蒸煮损失率,这与本试验结果一致。在不同的针间距下,蒸煮损失率在8 cm 处达到最大值。蒸煮损失率的原因很复杂,主要与热处理过程中肌原纤维蛋白的热变性程度有关。从表1可以看出,高压电场解冻过程中牛肉的离心损失率明显低于对照组(P<0.05)。这表明高压电场可以减少解冻过程中对牛肉细胞的损害而引起的水分流失。在不同的针间距下,离心损失率在8 cm 处达到最大值。离心损失率与汁液流失率密切相关。
表1 针间距对汁液流失率、蒸发损失率、蒸煮损失率和牛肉总损失率的影响
Table 1 Influence of needle spacing on the drip loss,evaporation loss,cooking loss and total loss of beef
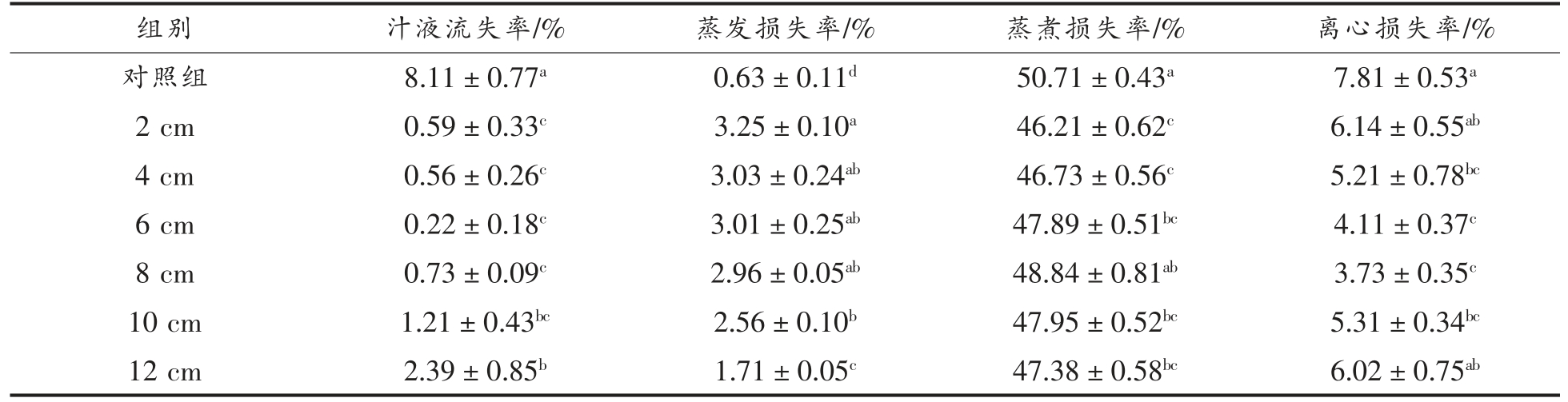
注:数据显示为“平均值±标准差”,字母代表均值存在显著性差异(P<0.05)。
?
2.3 颜色的测量结果
解冻牛肉样品的表面颜色通过测量其亮度(L*)、红色(a*)和黄色(b*)数值进行表达。图4为在高压电场作用下牛肉解冻后表面的颜色变化。L0*、a0*和b0*分别是对照组的亮度、红色和黄色。Li*、ai*和bi*分别是在不同针距下的亮度、红色和黄色。L0*、a0*和b0*分别为29.43±0.47、18.13±0.43和7.07±0.12。从图4可以看出,牛肉表面的Li*/L0*、ai*/a0*和bi*/b0*存在显著性差异 (P<0.05)。Li*/L0*和bi*/b0*的值大于1。表明高压电场作用下牛肉的亮度(L*)和黄度(b*)大于对照组。随着解冻时间的延长,牛肉表面的水分将减少,导致L* 和b*值降低。在大多数情况下,ai*/a0*之比小于1。表明高压电场作用下牛肉的红度小于对照组。Holman等[32]指出,当a* 值等于或大于14.5 时,牛肉的颜色被认为可以接受(95%接受)。O3 是高压电场放电过程中的副产物,具有很强的氧化性。解冻过程中牛肉中的脱氧肌红蛋白容易被O3 氧化成肌红蛋白,导致肌红蛋白含量增加,进而引起a* 值降低[33]。颜色参数(L*、a*和b*值)在针间距为8 cm 处达到最大值。
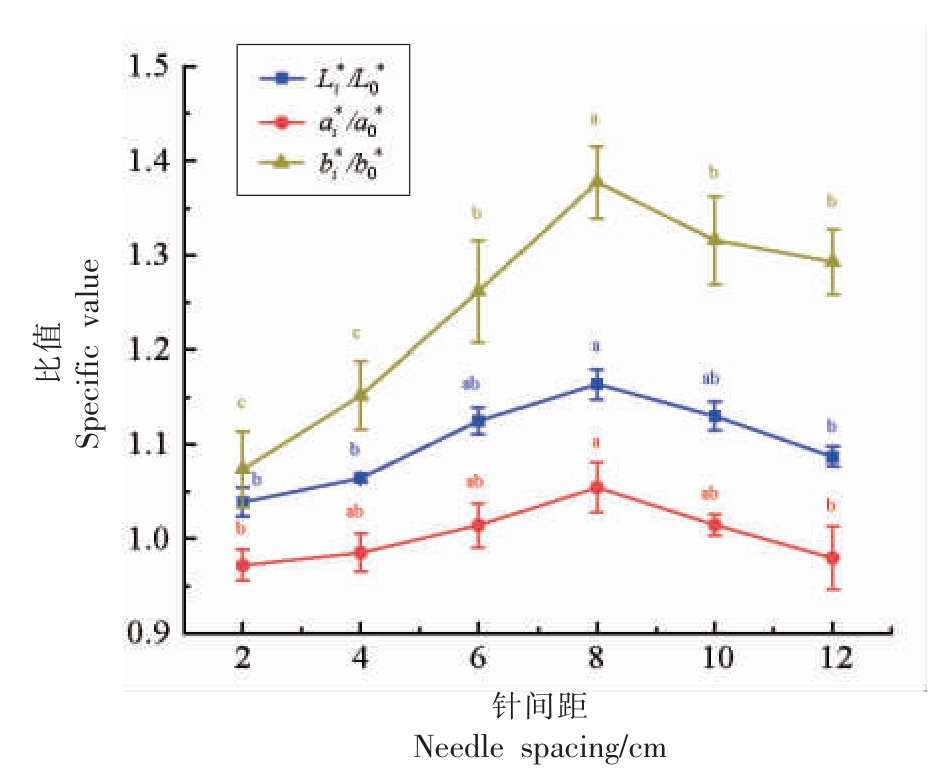
图4 不同针间距下解冻后牛肉的表面颜色变化动力学
Fig.4 Surface color change kinetics of thawed beef at different needle spacing
2.4 红外光谱的测量结果
图5为不同解冻条件下牛肉的红外光谱。经过查找资料,吸收峰归属如下:峰值在3 292.3 cm-1附近属于N-H 或O-H 的伸缩振动峰,2 923.1 cm-1附近属于C-H2 的不对称伸缩振动峰,2 852.9 cm-1附近属于C-H3 的对称拉伸振动峰,1 655.4 cm-1附近属于酰胺I 带,1 540.1 cm-1 附近属于酰胺II带,1 454.2 cm-1 附近属于C-H2 的弯曲振动峰,1 393.7 cm-1 附近属于C-H3 的对称变形振动峰,1 307.6 cm-1 和1 238.8 cm-1 附近属于酰胺III带,1 172 cm-1 附近属于C-H3 的摇摆振动峰,1 117.2 cm-1 附近属于C-C 的弯曲振动峰[34-37]。从图5可以看出,与对照组相比,不同高压电场处理组下的红外光图谱的特征峰的位置都比较接近,然而吸收峰强度不同。高压电场作用下牛肉的红外吸收峰明显高于对照组。说明高压电场解冻可以保存牛肉的营养成分,不同针间距处理组之间也存在差异。当针间距为6 cm 和8 cm 时,吸收峰强度高于其它组。当针间距为8 cm 时,牛肉解冻效果最佳。
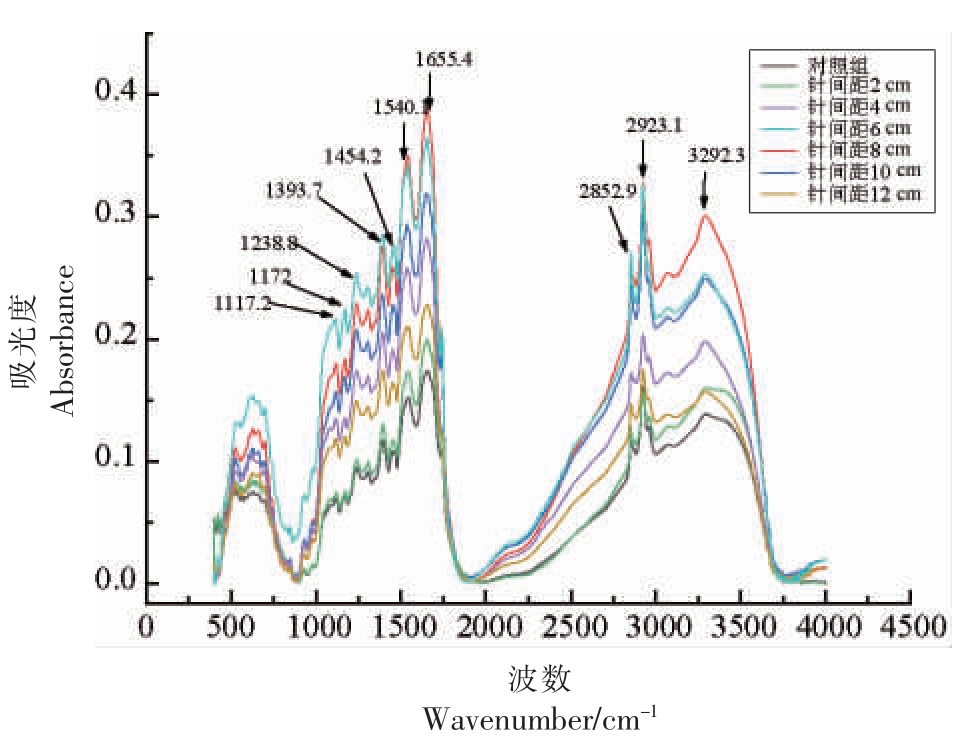
图5 不同解冻条件下牛肉的红外光谱
Fig.5 Infrared spectrum spectra of beef under different thawing conditions
2.5 共有峰率与变异峰率双指标序列分析的测量结果
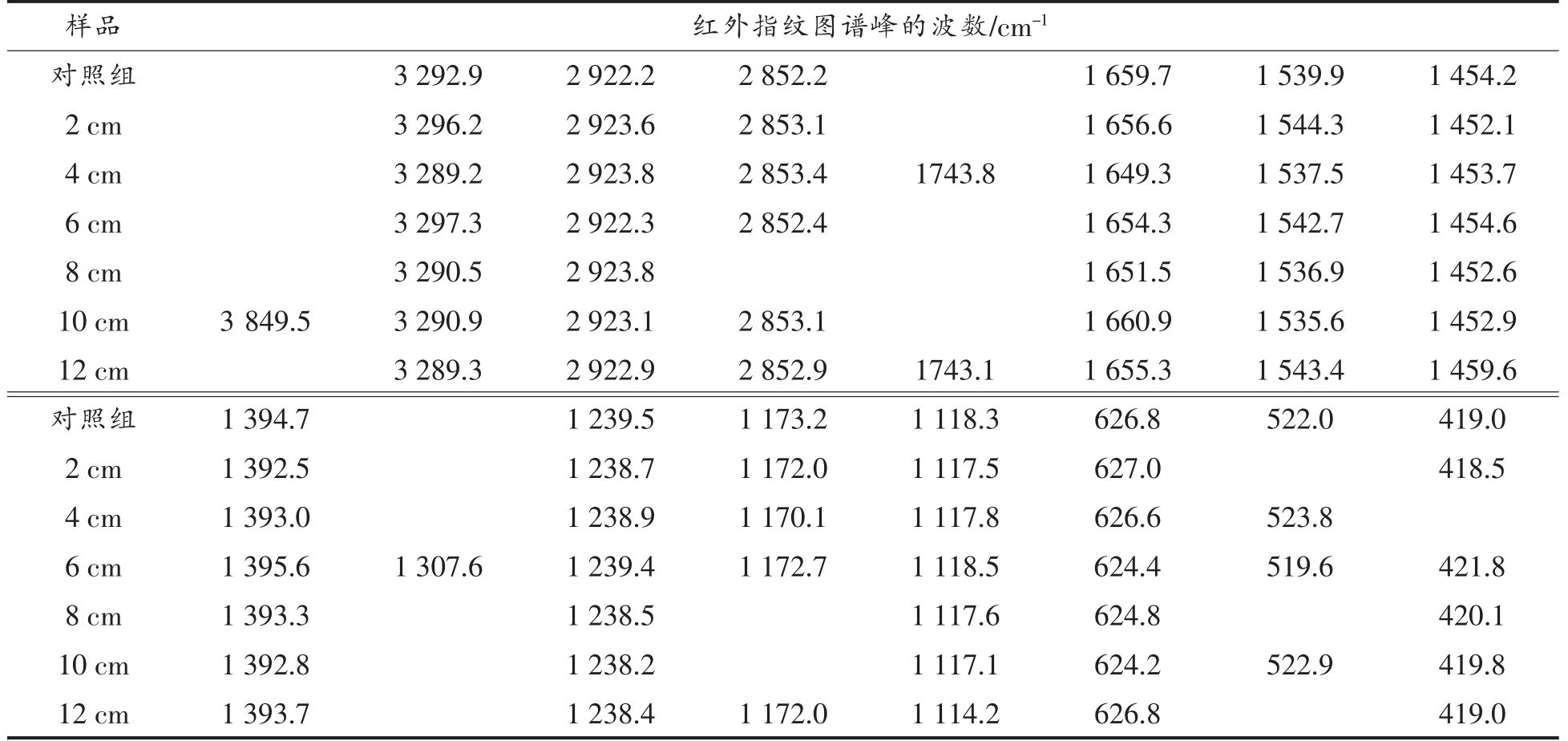
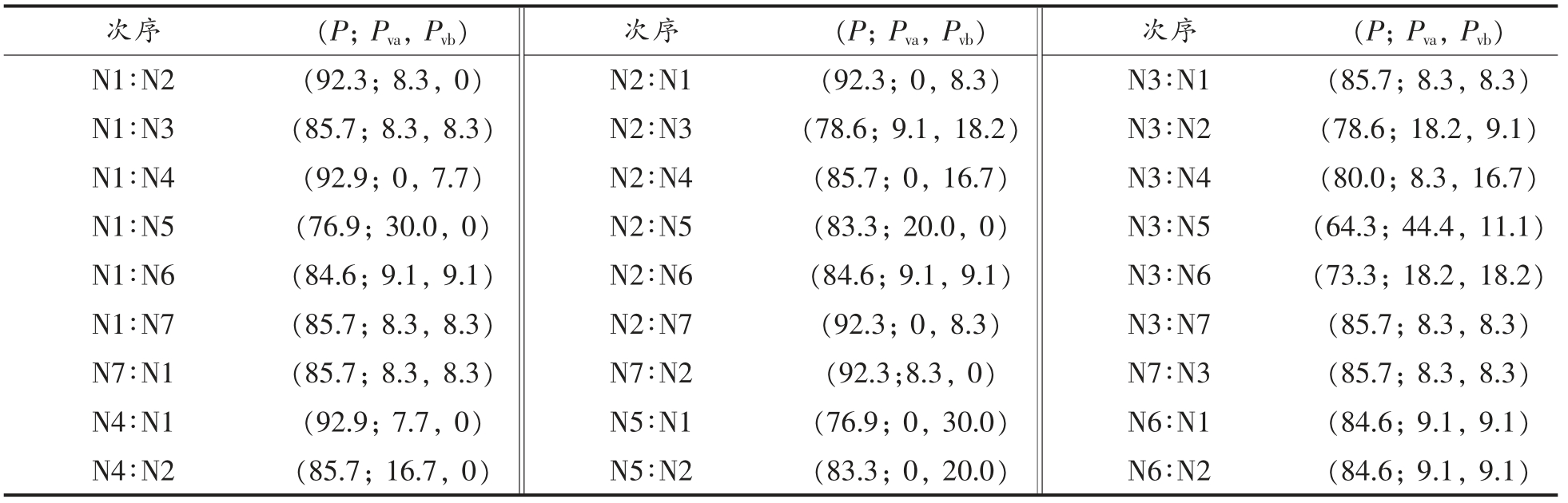
表2为在不同解冻条件下牛肉红外指纹图谱的吸收峰的波数。根据确定共有峰的方法,可以从表2中找到多组共有峰。对于其中一组峰(1 659.7,1 656.6,1 649.3,1 654.3,1 654.3,1 651.5,1 660.9,1 655.3 cm-1),平均波数为1 655.4 cm-1,该组峰的最大波数差为11.6 cm-1。该组峰与其前、后相邻组峰的平均波数差值分别为88.1 cm-1 和115.4 cm-1,波数差明显大于11.6 cm-1,可以判断该组峰是一组共有峰。表3为在不同针间距条件下牛肉红外指纹图谱的双索引序列分析。使用共有峰率和变异峰率的双指标,可以共性和差异两个方面全面刻画两个指纹图谱。共有峰率越高,两个指纹图谱的共性越大。变异峰率的变化越大,说明不同针间距的影响越大。
表2 不同针距下牛肉红外指纹图谱的吸收峰波数
Table 2 Wavenumbers of absorption peaks of beef infrared fingerprints under different needle spacings
样品 红外指纹图谱峰的波数/cm-1对照组 3 292.9 2 922.2 2 852.2 1 659.7 1 539.9 1 454.2 2 cm 3 296.2 2 923.6 2 853.1 1 656.6 1 544.3 1 452.1 4 cm 3 289.2 2 923.8 2 853.4 1743.8 1 649.3 1 537.5 1 453.7 6 cm 3 297.3 2 922.3 2 852.4 1 654.3 1 542.7 1 454.6 8 cm 3 290.5 2 923.8 1 651.5 1 536.9 1 452.6 10 cm 3 849.5 3 290.9 2 923.1 2 853.1 1 660.9 1 535.6 1 452.9 12 cm 3 289.3 2 922.9 2 852.9 1743.1 1 655.3 1 543.4 1 459.6对照组 1 394.7 1 239.5 1 173.2 1 118.3 626.8 522.0 419.0 2 cm 1 392.5 1 238.7 1 172.0 1 117.5 627.0 418.5 4 cm 1 393.0 1 238.9 1 170.1 1 117.8 626.6 523.8 6 cm 1 395.6 1 307.6 1 239.4 1 172.7 1 118.5 624.4 519.6 421.8 8 cm 1 393.3 1 238.5 1 117.6 624.8 420.1 10 cm 1 392.8 1 238.2 1 117.1 624.2 522.9 419.8 12 cm 1 393.7 1 238.4 1 172.0 1 114.2 626.8 419.0
表3 不同解冻条件下牛肉红外指纹图谱的双指标序列分析
Table 3 Double-index sequences analysis of beef infrared fingerprints under different thawing conditions
次序 (P;Pva,Pvb) 次序 (P;Pva,Pvb) 次序 (P;Pva,Pvb)N1∶N2 (92.3;8.3,0) N2∶N1 (92.3;0,8.3) N3∶N1 (85.7;8.3,8.3)N1∶N3 1∶N4 (85.7;8.3,8.3) N2∶N3 (78.6;9.1,18.2) N3∶N2 (78.6;18.2,9.1)N(92.9;0,7.7) N2∶N4 (85.7;0,16.7) N3∶N4 (80.0;8.3,16.7)N1∶N5 (76.9;30.0,0) N2∶N5 (83.3;20.0,0) N3∶N5 (64.3;44.4,11.1)N1∶N6 (84.6;9.1,9.1) N2∶N6 (84.6;9.1,9.1) N3∶N6 (73.3;18.2,18.2)N1∶N7 (85.7;8.3,8.3) N2∶N7 (92.3;0,8.3) N3∶N7 (85.7;8.3,8.3)N7∶N1 (85.7;8.3,8.3) N7∶N2 (92.3;8.3,0) N7∶N3 (85.7;8.3,8.3)N4∶N1 (92.9;7.7,0) N5∶N1 (76.9;0,30.0) N6∶N1 (84.6;9.1,9.1)N4∶N2 (85.7;16.7,0) N5∶N2 (83.3;0,20.0) N6∶N2 (84.6;9.1,9.1)
(续表3)
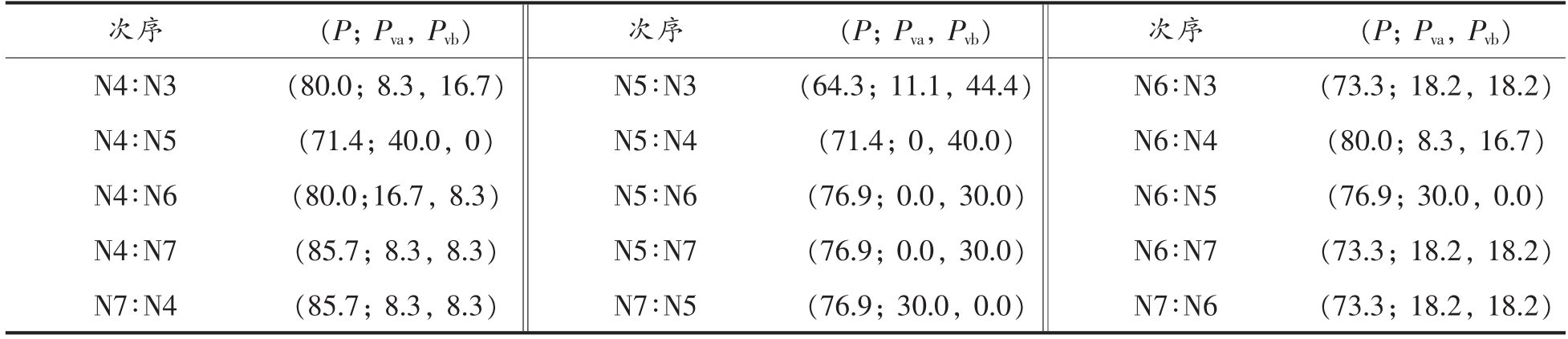
注:N.对照组;N2.2 cm;N3.4 cm;N4.6 cm;N5.8 cm;N6.10 cm;N7.12 cm。
?
A 组:N1∶N4 (92.9;0,7.7),N4∶N1(92.9;7.7,0);N1∶N2(92.3;8.3,0),N2∶N1(92.3;0,8.3);N2∶N7(92.3;0,8.3),N7∶N2(92.3;8.3,0)。
B 组:N3∶N5 (64.3;44.4,11.1),N5∶N3(64.3;11.1,44.4);N4∶N5(71.4;40.0,0),N5∶N4(71.4;0,40.0)。
在A 组中,N1 和N4,N1 和N2,N2 和N7 具有最高的共有峰率和最小的变异峰率,因此具有最高的相似性。表明当针间距为2,6,12 cm 时,高压电场具有相似的作用。在不同解冻条件下,针间距为6 cm 时与对照组具有最高的相似性。在B 组中,N3 和N5,N4 和N5 具有非常低的共有峰率和非常高的变异峰率。表明当针间距为8 cm 时,高压电场对牛肉的内部成分影响与对照组相比是最大的。从以上分析可以看出,在不同的针间距下,高压电场对牛肉内部成分的影响不同。这些分析正确反映了实际情况,与本试验结果相似。
2.6 蛋白质二级结构的测量结果
图6显示了不同针间距的酰胺I 带(1 600~1 700 cm-1)的红外光谱图曲线拟合结果。距报道,酰胺I 带的形状用于确定蛋白质二级结构,其位于1 600~1 700 cm-1[24]。各子峰与二级结构之间的对应关系如下:1 610~1 642 cm-1 是β-折叠,1 642~1 650 cm-1 是无规卷曲,1 650~1 660 cm-1 是α-螺旋,1 660~1 680 cm-1 是β-转角,1 680~1 700 cm-1 是β-反平行折叠[38]。α-螺旋和β-折叠(平行和反平行)是有序结构的代表。β-转角和无规卷曲是无序结构的代表[39]。从图6中可以看出,在2,4,6,8,10,12 cm 和对照组,有序结构的含量分别为65.68%,59.65%,61.97%,61.10%,73.56%,61.91%和68.79%。在2,4,6,8,10,12 cm 和对照组,无序结构的含量分别为33.57%,40.36%,37.22%,37.2%,26.45%,38.1%和30.51%。α-螺旋和β-折叠通过肽链之间的氢键维持,氢键是稳定二级结构的主要作用力。高压电场会影响牛肉的微观结构,氢键作用减弱,导致α-螺旋和β-折叠破裂,形成无规卷曲和β-转角。Zhang 等[40]研究了高压对鸡胸肉的影响,发现α-螺旋和β-折叠的有序结构减少,β-转角和无规卷曲的无序结构增加。这表明高压产生的能量将导致蛋白质解开并削弱氢键,从而导致有序结构被破坏。
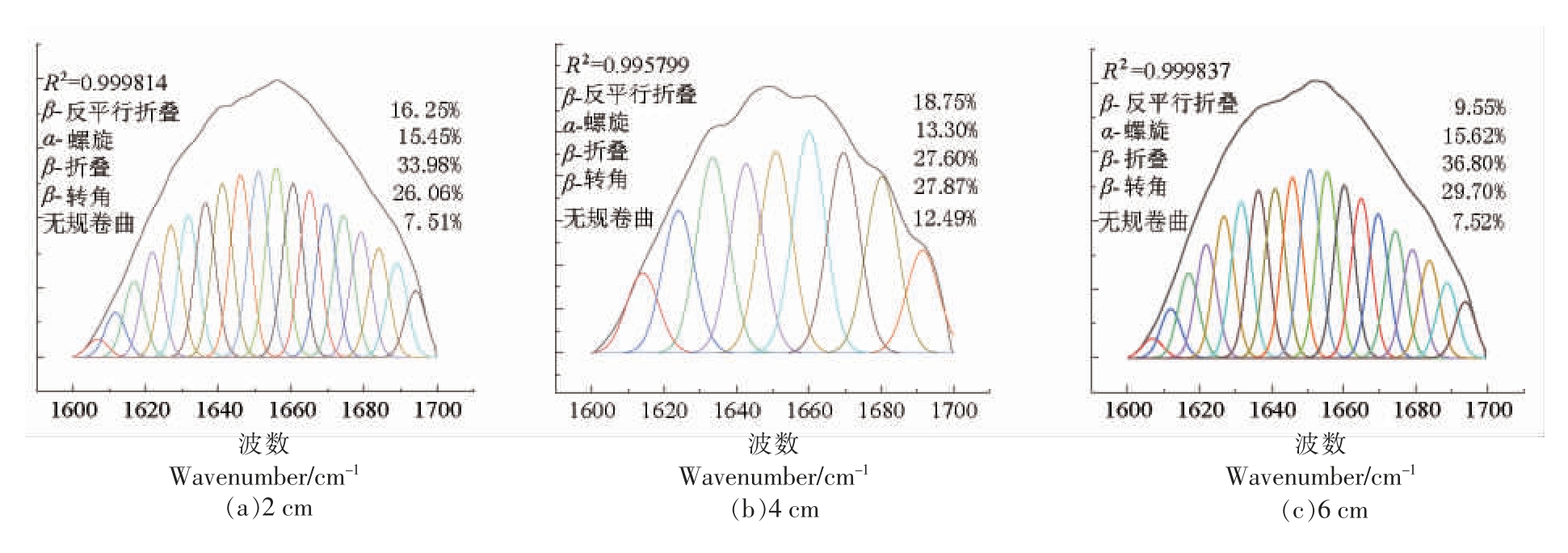
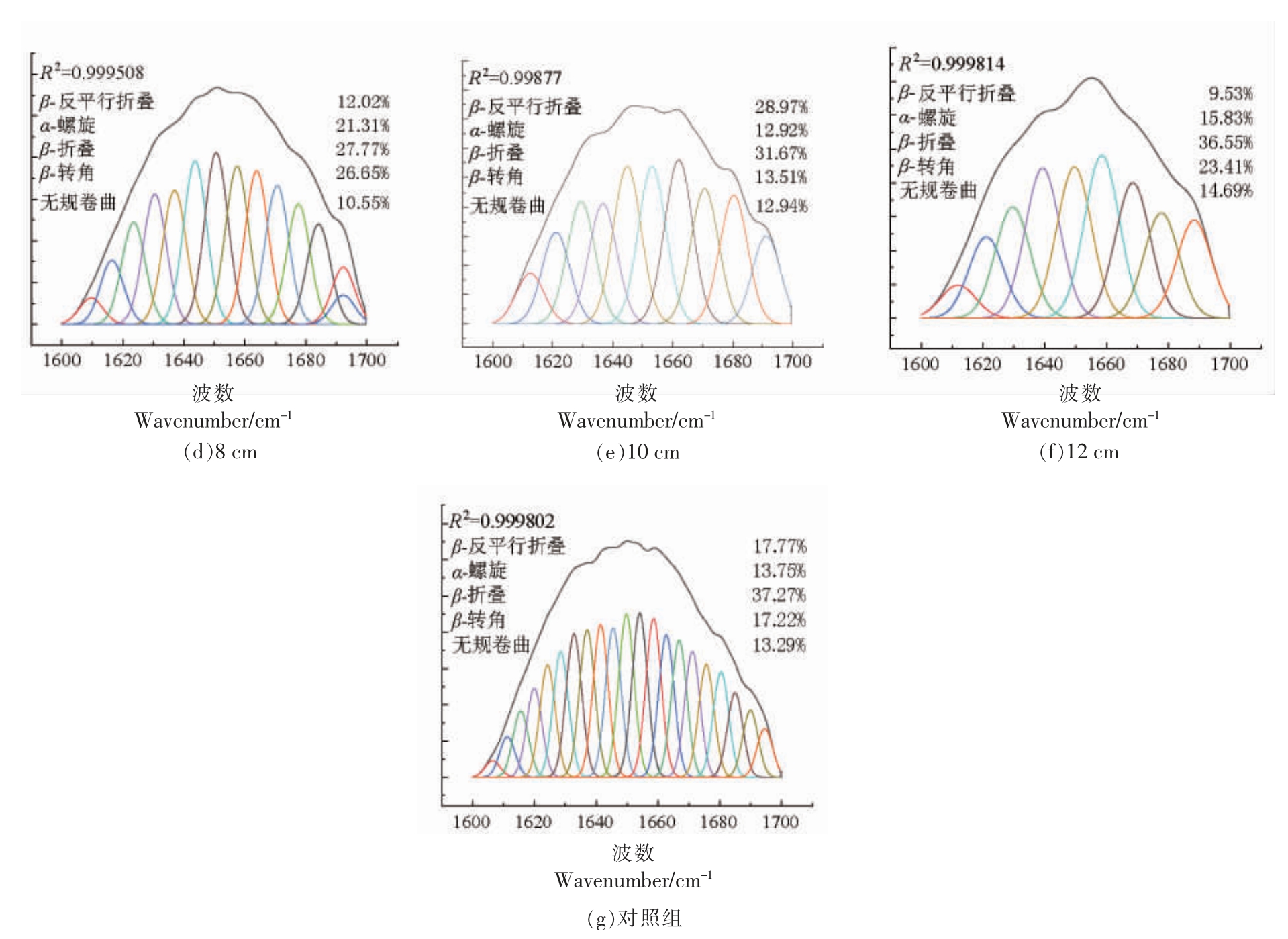
图6 不同针间距下牛肉的酰胺I 带(1 600~1 700 cm-1)的红外光谱图曲线拟合结果
Fig.6 The infrared spectrum spectrograms and curve-fitting results of amide I band for beef of the different needle spacings in the range of 1 600-1 700 cm-1
3 结论
高压电场作用下牛肉的解冻速率和蒸发损失率均显著高于对照组,解冻时间、汁液流失率、蒸煮损失率和离心损失率均显著低于对照组。不同针间距处理组的牛肉红外光谱的吸收峰强度随针间距的增加呈一定规律性。红外指纹图谱的共有峰率和变异峰率的双指标序列分析表明,高压电场解冻在4,6,8 cm 处对牛肉有一定程度的影响。蛋白质二级结构分析结果表明,高压电场可以降低α-螺旋和β-折叠的有序结构,增加β-转角和无规卷曲的无序结构。
[1]CAI L,ZHANG W,CAO A,et al.Effects of different thawing methods on the quality of largemouth bass (Micropterus salmonides)[J].LWT-Food Science and Technology,2020,120:108908.
[2]EASTRIDGE J S,BOWKER B C.Effect of rapid thawing on the meat quality attributes of USDA select beef strip loin steaks[J].Journal of Food Science,2011,76(2):156-162.
[3]ERSOY B,AKSAN E,OZEREN A.The effect of thawing methods on the quality of eels (Anguilla anguilla)[J].Food Chemistry,2008,111(2):377-380.
[4]XIA X,KONG B,LIU J,et al.Influence of different thawing methods on physicochemical changes and protein oxidation of porcine longissimus muscle[J].LWT-Food Science and Technology,2012,46(1):280-286.
[5]CAO M,CAO A,WANG J,et al.Effect of magnetic nanoparticles plus microwave or far-infrared thawing on protein conformation changes and moisture migration of red seabream (Pagrus Major) fillets[J].Food Chemistry,2018,266:498-507.
[6]CAI L,CAO M,REGENSTEIN J,et al.Recent advances in food thawing technologies[J].Comprehensive Reviews in Food Science and Food Safety,2019,18(4):953-970.
[7]HE X,JIA G,TATSUMI E,et al.Effect of corona wind,current,electric field and energy consumption on the reduction of the thawing time during the high-voltage electrostatic-field (HVEF) treatment process[J].Innovative Food Science & Emerging Technologies,2016,34:135-140.
[8]JIA G,KUN S,JIN M,et al.Effect of high voltage electrostatic field treatment on thawing characteristics and post-thawing quality of lightly salted,frozen pork tenderloin[J].LWT-Food Science and Technology,2019,99:268-275.
[9]RAHBARI M,HAMDAMI N,MIRZAEI H,et al.Effects of high voltage electric field thawing on the characteristics of chicken breast protein[J].Journal of Food Engineering,2018,216:98-106.
[10]LI D,JIA S,ZHANG L,et al.Post-thawing quality changes of common carp (Cyprinus carpio) cubes treated by high voltage electrostatic field (HVEF)during chilled storage[J].Innovative Food Science &Emerging Technologies,2017,42:25-32.
[11]HE X,LIU R,NIRASAWA S,et al.Effect of high voltage electrostatic field treatment on thawing characteristics and post-thawing quality of frozen pork tenderloin meat [J].Journal of Food Engineering,2013,115(2):245-250.
[12]HE X,LIU R,TATSUMI E,et al.Factors affecting the thawing characteristics and energy consumption of frozen pork tenderloin meat using high-voltage electrostatic field[J].Innovative Food Science &Emerging Technologies,2014,22:110-115.
[13]MOUSAKHANI-GANJEH A,HAMDAMI N,SOLTANIZADEH N.Impact of high voltage electric field thawing on the quality of frozen tuna fish(Thunnus albacares)[J].Journal of Food Engineering,2015,156:39-44.
[14]MOUSAKHANI-GANJEH A,HAMDAMI N,SOLTANIZADEH N.Effect of high voltage electrostatic field thawing on the lipid oxidation of frozen tuna fish (Thunnus albacares)[J].Innovative Food Science and Emerging Technologies,2016,36:42-47.
[15]AMIRI A,MOUSAKHANI-GANJEH A,SHAFIEKHANI S,et al.Effect of high voltage electrostatic field thawing on the functional and physicochemical properties of myofibrillar proteins[J].Innovative Food Science & Emerging Technologies,2019,56:102191.
[16]BUREAU S,COZZOLINO D,CLARK C J.Contributions of Fourier-transform mid infrared (FT-MIR)spectroscopy to the study of fruit and vegetables:A review[J].Postharvest Biology and Technology,2019,148:1-14.
[17]蔡健荣,万新民,陈全胜.近红外光谱法快速检测猪肉中挥发性盐基氮的含量[J].光学学报,2009,29(10):2808-2812.
CAI J R,WAN X M,CHEN Q S.Feasibility study for the use of near-infrared spectroscopy in the quantitative analysis of TVB-N content in pork[J].Acta Optica Sinica,2009,29(10):2808-2812.
[18]ZHUANG H,NI Y,KOKOT S.A comparison of near-and mid-infrared spectroscopic methods for the analysis of several nutritionally important chemical substances in the Chinese yam (Dioscorea opposita):Total sugar,polysaccharides,and flavonoids[J].Applied Spectroscopy,2015,69(4):488-495.
[19]ACRI G,TESTAGROSSA B,VERMIGLIO G.FTNIR analysis of different garlic cultivars[J].Journal of Food Measurement and Characterization,2016,10(1):127-136.
[20]NI J,DING C,ZHANG Y,et al.Impact of different pretreatment methods on drying characteristics and microstructure of goji berry under electrohydrodynamic (EHD) drying process[J].Innovative Food Science and Emerging Technologies,2020,61:102318.
[21]ALIZADEH E,CHAPLEAU N,DE LAMBALLERIE M,et al.Effects of freezing and thawing processes on the quality of Atlantic salmon (Salmo salar) Fillets[J].Journal of Food Science,2007,72(5):279-284.
[22]LI C,WANG D,XU W,et al.Effect of final cooked temperature on tenderness,protein solubility and microstructure of duck breast muscle[J].LWT-Food Science and Technology,2013,51(1):266-274.
[23]LI D,JIA S,ZHANG L,et al.Effect of using a high voltage electrostatic field on microbial communities,degradation of adenosine triphosphate,and water loss when thawing lightly-salted,frozen common carp (Cyprinus carpio)[J].Journal of Food Engineering,2017,212:226-233.
[24]周晔,张庆伟,罗学军,等.傅里叶红外光谱法鉴别部分胡椒属生药的研究[J].光谱学与光谱分析,2014,34(9):2419-2423.
ZHOU Y,ZHANG Q W,LUO X J,et al.Identification of some piper crude drugs based on Fourier transform infrared spectrometry[J].Spectroscopy and Spectral Analysis,2014,34(9):2419-2423.
[25]CARBONARO M,NUCARA A.Secondary structure of food proteins by Fourier transform spectroscopy in the mid-infrared region[J].Amino Acids,2010,38(3):679-690.
[26]BOONSUMREJ S,CHAIWANICHSIRI S,TANTRATIAN S,et al.Effects of freezing and thawing on the quality changes of tiger shrimp (Penaeus monodon) frozen by air-blast and cryogenic freezing[J].Journal of Food Engineering,2007,80(1):292-299.
[27]MARTYNENKO A,KUDRA T,YUE J.Multipin EHD dryer:Effect of electrode geometry on charge and mass transfer[J].Drying Technology,2017,35(16):1970-1980.
[28]HUFF-LONERGAN E,LONERGAN S M.Mechanisms of water-holding capacity of meat:The role of postmortem biochemical and structural changes[J].Meat Science,2005,71(1):194-204.
[29]LEYGONIE C,BRITZ T J,HOFFMAN L C.Impact of freezing and thawing on the quality of meat:Review[J].Meat Science,2012,91(2):93-98.
[30]OTTO G,ROEHE R,LOOFT H,et al.Drip loss of case-ready meat and of premium cuts and their associations with earlier measured sample drip loss,meat quality and carcass traits in pigs[J].Meat Science,2006,72(4):680-687.
[31]HSIEH C W,LAI C H,HO W J,et al.Effect of thawing and cold storage on frozen chicken thigh meat quality by high-voltage electrostatic field[J].Journal of Food Science,2010,75(4):193-197.
[32]HOLMAN B W,VAN DE VEN R J,MAO Y,et al.Using instrumental (CIE and reflectance) measures to predict consumers' acceptance of beef colour[J].Meat Science,2017,127:57-62.
[33]JALARAMA R K,JAYATHILAKAN K,CHAUHAN O P,et al.Effect of high-pressure processing on physico-chemical and microbial quality characteristics of chevon (Capra aegagrus hircus)[J].Food and Bioprocess Technology,2015,8(12):2347-2358.
[34]CHEN Q,ZHANG Y,GUO Y,et al.Non-destructive prediction of texture of frozen/thaw raw beef by Raman spectroscopy[J].Journal of Food Engineering,2020,266:109693.
[35]CHEN Y,ZOU C,MASTALERZ M,et al.Applications of micro-Fourier transform infrared spectroscopy (FTIR) in the geological sciences--A review[J].International Journal of Molecular Sciences,2015,16(12):30223-30250.
[36]ZHAO M,DOWNEY G,O'DONNELL C P.Exploration of microwave dielectric and near infrared spectroscopy with multivariate data analysis for fat content determination in ground beef[J].Food Control,2016,68:260-270.
[37]吕慧茹,欧全宏,刘刚,等.不同品质宣威火腿的傅里叶变换红外光谱研究[J].光学学报,2015,35(z2):247-251.
LV H R,OU Q H,LIU G,et al.Study of different quality Xuanwei hams by Fourier transform infrared spectroscopy[J].Acta Optica Sinica,2015,35(z2):247-251.
[38]HE S,SHI J,WALID E,et al.Reverse micellar extraction of lectin from black turtle bean (Phaseolus vulgaris):Optimisation of extraction conditions by response surface methodology[J].Food Chemistry,2015,166:93-100.
[39]QIAN S,LI X,WANG H,et al.Effects of low voltage electrostatic field thawing on the changes in physicochemical properties of myofibrillar proteins of bovine longissimus dorsi muscle[J].Journal of Food Engineering,2019,261:140-149.
[40]ZHANG Z,YANG Y,ZHOU P,et al.Effects of high pressure modification on conformation and gelation properties of myofibrillar protein[J].Food Chemistry,2017,217:678-686.