孕产期女性受激素等因素影响,其身体和心理发生重大变化[1]。母乳是婴幼儿最理想的食物来源,母乳成分受母亲膳食影响。临床研究发现母体在孕期补充乳酸双歧杆菌动物菌株HNO19,可以在初乳和3 个月的母乳中检测到同株菌[2]。母乳中的微生物可以传递给婴儿,如双歧杆菌、乳酸杆菌等,可抑制病原微生物在婴儿肠道内生长定植,促进婴儿肠道微生态健康[3-6]。纯母乳喂养方式下,母乳中蛋白质、脂肪等主要营养物质含量可能直接影响婴幼儿早期生长发育[7],母乳里的蛋白质可以促进2~12 周的婴幼儿的生长速率[8]。有研究表明膳食干预会影响母乳中的脂肪、干物质和总能量[9]。然而,由于膳食干预对母乳成分的影响不显著,使用益生菌干预母乳成分逐渐成为学者们争相探究的课题。
益生菌是指活的微生物,当量足够大时,会赋予宿主健康益处。有研究以肥胖大鼠作为试验对象,发现嗜酸乳杆菌及短双歧杆菌均能一定程度上改善肥胖大鼠的肥胖指数、血脂紊乱及胰岛素抵抗[10]。Park 等[11]研究发现,植物乳杆菌HAC01 通过调节毛罗菌科和瘤胃菌科,减轻肥胖小鼠脂肪堆积,上调脂质氧化相关基因的表达。此外,临床研究也显示,益生菌能有效调节肥胖患者的体质量,嗜黏蛋白阿克曼氏菌能够改善肠道屏障功能,调节高脂饮食相关的代谢紊乱,如体重增加、代谢性内毒素血症、脂肪组织炎症及胰岛素抵抗等[12]。对于婴幼儿而言,母亲孕期增重过多也可能导致学龄前儿童发生超重或肥胖[13]。益生元的最新定义为:一种可以被宿主微生物选择性利用,从而赋予健康益处的基质[14],包括低聚果糖、低聚半乳糖、菊粉等[15]。目前常见的益生元包括乳果糖、低聚果糖。益生元能够增加饱腹感和降低食欲[16],能够被人体肠道益生菌发酵利用,增加原籍益生菌,遏制有害菌,减低机体炎症状态,改善糖脂代谢,调节肠道激素变化,从而改善肥胖及肥胖相关代谢紊乱[17],是超重或肥胖人群控制体重的理想选择。
抑郁症是当今世界最常见的精神障碍,具有显著持久的心境低落、兴趣减退和快感缺失等临床特征[18],在全球的发生率高达10%~30%[19]。研究发现产后抑郁和婴幼儿心理行为发育的关系呈正比[20],对婴儿体格发育和发育商有负面影响的可能[21]。另外,产后抑郁还是婴幼儿社会情绪能力发展不良的重要风险因素[22]。为了提高产后母子精神健康水平,研究人员们发现给予幼年大鼠益生菌,能够改善亲子分离应激模型小鼠抑郁症状,且有益效应延续到小鼠成年以后,用益生菌调节胃肠功能同样能改善临床患者的抑郁症状[23-24]。瑞士乳杆菌R0052 和长双岐杆菌R0175 也可以改善抑郁焦虑症状[25]。此外,有证据证明益生元通过推动有益微生物的生长,改善焦虑、抑郁症状[26]。
有关益生菌、益生元对超重肥胖孕妇的影响已有部分报道,然而,不同菌株或其组合与代谢物具有不同功效,目前缺少益生菌孕产期干预对母子健康功效的研究。本文探究既富含益生菌,又富含益生元的发酵乳对母乳成分、母子身体和心理健康水平的影响。
1 材料与方法
1.1 受试者纳入及排除标准
纳入标准:年龄18~35 岁;单胎妊娠;入组孕周8~12 周零6 天 (根据末次月经或B 超监测);BMI≥25 kg/m2,在京居住至少5年,无孕前高血压、糖尿病、高脂血症、肝炎、肾炎、消化道疾病(慢性胃炎、肠炎、胃溃疡及十二指肠溃疡等)及感染性疾病史(肝炎、肺结核等)。
排除标准:近1 个月服用抗生素、益生菌或益生元,规律吸烟、饮酒,辅助生育技术受孕,精神类疾病不能正确回答问题或不愿进行问卷调查者不纳入本研究;减肥手术史;不能依从膳食推荐;乳糖不耐受;牛奶蛋白过敏。
1.2 受试者招募、干预与跟踪
招募Y(发酵乳组)84、C(对照组)62 名受试者(产妇),研究获得首都医科大学附属北京地坛医院医学伦理委员会批准(2017-KY-015-02),所有志愿者签署知情同意书,每日饮用一瓶富含益生菌益生元的衡安堂166 发酵乳(简称166 发酵乳)200 mL。166 发酵乳配料如下:生牛乳、菊粉(1%~2%,质量分数,下同)、低聚果糖(1%~2%)、聚葡萄糖(≤1%)、低聚异麦芽糖(≤1%)、低聚半乳糖(1%~2%)、低聚木糖(≤1%)、甜菊糖苷、罗汉果甜苷、格氏乳杆菌、嗜热链球菌、保加利亚乳杆菌、嗜酸乳杆菌(Lactobacillus acidophilus)、植物乳杆菌(Lactobacillus plantarum)、副干酪乳杆菌(Lactobacillus paracasei)、短双岐杆菌(Bifidobacterium breve)、乳双歧杆菌(Bifidobacterium lactobacillus)、长双歧杆菌(Bifidobacterium longum)。
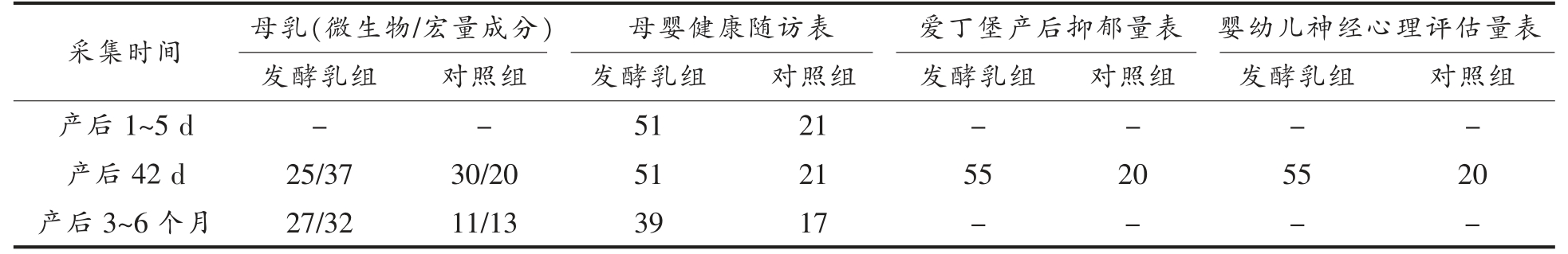
分别在产后1~5 d,42±3 d,3~6 个月收集采集母乳;产后42 d 收集母婴健康随访表、婴幼儿神经心理评估量表ASQ-3、爱丁堡产后抑郁量表(Edinburgh Postnatal Depression Scale,EPDS)。母乳采集方法:用香皂或洗手液洗净双手,并用干净的湿巾轻轻擦拭乳头及乳晕,上午9:00-11:00 用消毒后的吸奶器吸空一侧乳房乳汁,将前乳和后乳混匀后取10 毫升于无菌的离心管中,采集后暂时存放在-20 ℃冰箱中,24 h 内低温转移到-80 ℃冰箱。受疫情影响,各阶段有部分受试者退组以及个别信息缺填情况。由于初乳采集量较少,而母乳成分和微生物分析样本用量较高,因此没有对初乳进行检测与分析;产后6 周内是抑郁症的高发期[27],以产后42 d 为代表分析发酵乳干预对产后近期母婴健康、产妇抑郁、婴幼儿神经心理发育的影响。各阶段采集的样本数量及量表收集数量见表1。
表1 样本及量表采集数量
Table 1 Number of collected samples and scales
?
1.3 样本检测和健康评估量表
母乳微生物检测:采用CTAB 或SDS 法提取母乳样本基因组DNA,使用琼脂糖凝胶电泳检测DNA 的浓度和纯度,然后对母乳菌群16S rRNA V3-V4 区进行聚合酶链式反应扩增,扩增引物为515F-806R,位于16S V4 区,扩增产物由2%浓度的琼脂糖凝胶电泳检测,然后使用Qiagen 公司提供的胶回收试剂盒进行纯化,利用Illumina 公司TruSeq® DNA PCR-Free Sample Preparation Kit建库试剂盒进行文库构建,构建好文库后,通过Qubit 和Q-PCR 定量,最后通过NovaSeq6000 进行上机测序。
母乳宏量成分检测:首先使用3 mL 加热至40 ℃的CLEAN 液对Miris HMA 母乳分析仪进行清洗,注入3 mL 的CHECK 液进行指标校正。接着使用离心管取3~5 mL 的母乳样本进行超声,再使用5 mL 规格注射器将样本注入母乳分析仪中,检测完成之后进行仪器清洗,防止影响下次使用。
母子健康指标:母亲身体质量指数(Body Mass Index,BMI)、婴幼儿体重增长指标,通过爱丁堡产后抑郁量表、婴幼儿神经心理评估量表ASQ-3 分别评估产妇、婴幼儿神经心理发育状况。
1.4 统计分析
采用SPSS 19.0 软件统计分析,计量资料以( ±s)形式表示,采用独立样本t 检验,计数资料比较采用卡方检验,检验水准以P<0.05 表示数据比较结果差异有统计学意义。
±s)形式表示,采用独立样本t 检验,计数资料比较采用卡方检验,检验水准以P<0.05 表示数据比较结果差异有统计学意义。
对比两组母亲的身体质量指数(BMI)、爱丁堡产后抑郁量表(EPDS)得分等指标。
试验数据的分析处理以及图表绘制:SPSS,Oringin 等软件。
2 结果与分析
2.1 发酵乳干预对母乳菌群相对丰度的影响
从图1可以看出,在属水平上,对照组在产后42 d 以不动杆菌属(Acinetobacter)、葡萄球菌属(Staphylococcus)、链球菌属(Streptococcus)、假单胞菌属(Pseudomonas)、寡养单胞菌属(Stenotrophomonas)为优势菌属;发酵乳组以不动杆菌属、葡萄球菌属、假单胞菌属、链球菌属、沙雷氏菌属(Serratia)为优势菌属。在产后3~6 个月,对照组以不动杆菌属、葡萄球菌属、链球菌属、假单胞菌属、沙雷氏菌属为优势菌属;发酵乳组以不动杆菌属、葡萄球菌属、链球菌属、假单胞菌属、沙雷氏菌属为优势菌属。
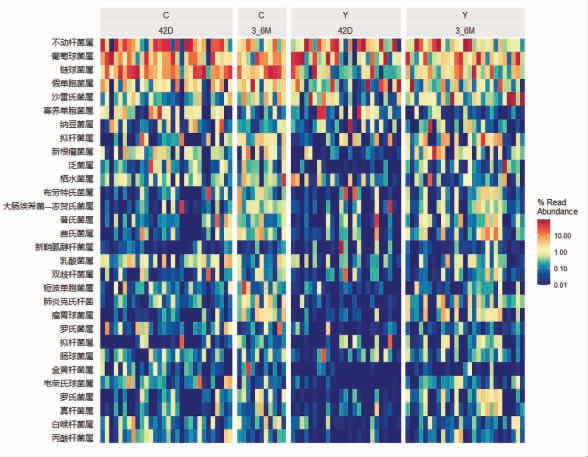
图1 发酵乳干预对产后42 d,3~6 个月母乳菌群属水平上相对丰度的影响
Fig.1 Effect of fermented dairy intervention on the relative abundance of breast milk flora at genus level on postpartum 42 days and 3-6 months
注C.对照组;Y.发酵乳组。
2.2 发酵乳干预对母乳菌群整体结构的影响
图2显示,在产后42 d,母乳菌群的群落构成具有显著差异 (P=0.001),且发酵乳组逐渐沿着PCo2(贡献率9.8%)拉开距离,同时也说明存在造成这种显著差异的关键菌属;在产后3~6 个月,发酵乳组和对照组的母乳微生物存在部分重合(P=0.885)。即发酵乳干预可以显著改变产后42 d 母乳微生物菌群的整体结构。
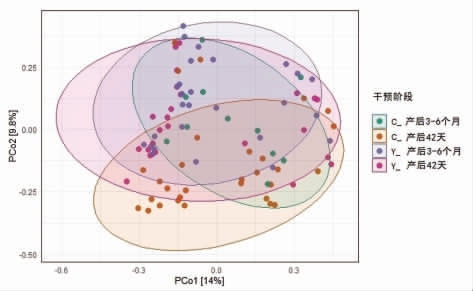
图2 PCoA 分析
Fig.2 PCoA analysis
注:C.对照组;Y.发酵乳组。
2.3 发酵乳组和对照组的差异菌属分析
将发酵乳组和对照组产后42 d、3~6 个月的母乳微生物比较发现,在属的水平上,与对照组相比,产后42 d 发酵乳组的罗尔斯通菌属(Ralstonia)、细球菌属(Micrococcaceae)显著上升;韦荣氏球菌属(Veillonella)、痤疮丙酸杆菌(Cutibacterium)、链球菌属、泛菌属(Pantoea)、兼性双球菌属(Gemella)、罗斯氏菌属 (Rothia)、奈瑟氏菌属(Neisseria)等菌属显著下降(P<0.05)(图3a)。在产后3~6 个月,经过发酵乳干预后,母乳中的细球菌属、大肠志贺氏杆菌(Escherichia-Shigella)、罕见小球菌属显著上升;链球菌属显著下降(P<0.05)(图3b)。
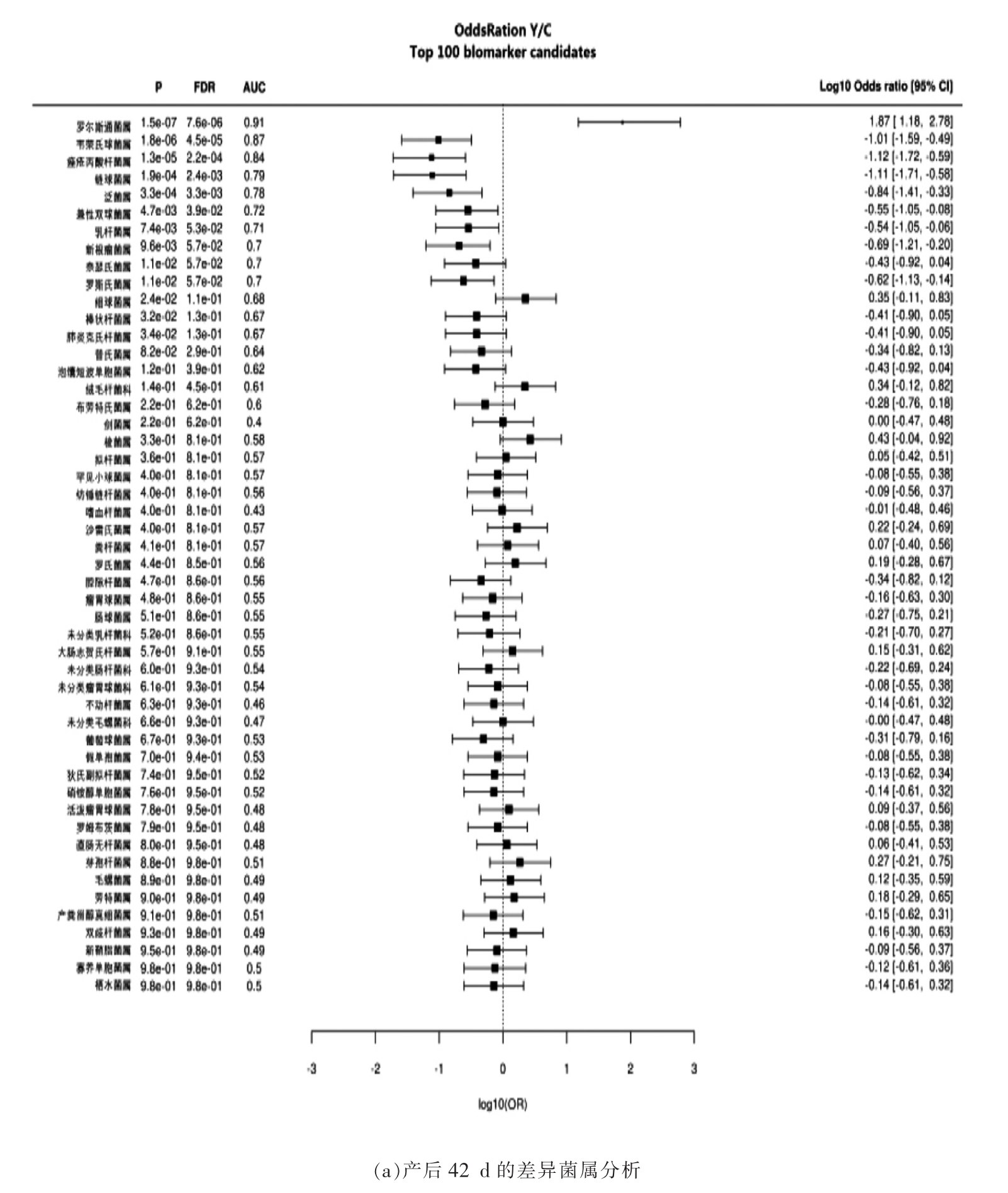

图3 母乳微生物的差异菌属分析
Fig.3 Differential bacteria analysis on dominant genus
2.4 发酵乳干预对母乳宏量成分的影响
根据发酵乳组和对照组在产后42 d 和产后3~6 个月两组母乳中的宏量成分比较分析,发现在脂肪、总蛋白、真蛋白、糖类、干物质以及总能量中,仅产后3~6 个月时,发酵乳组母乳中的真蛋白含量显著高于对照组(P=0.033),其它宏量成分在两组中无统计学差异(图4)。
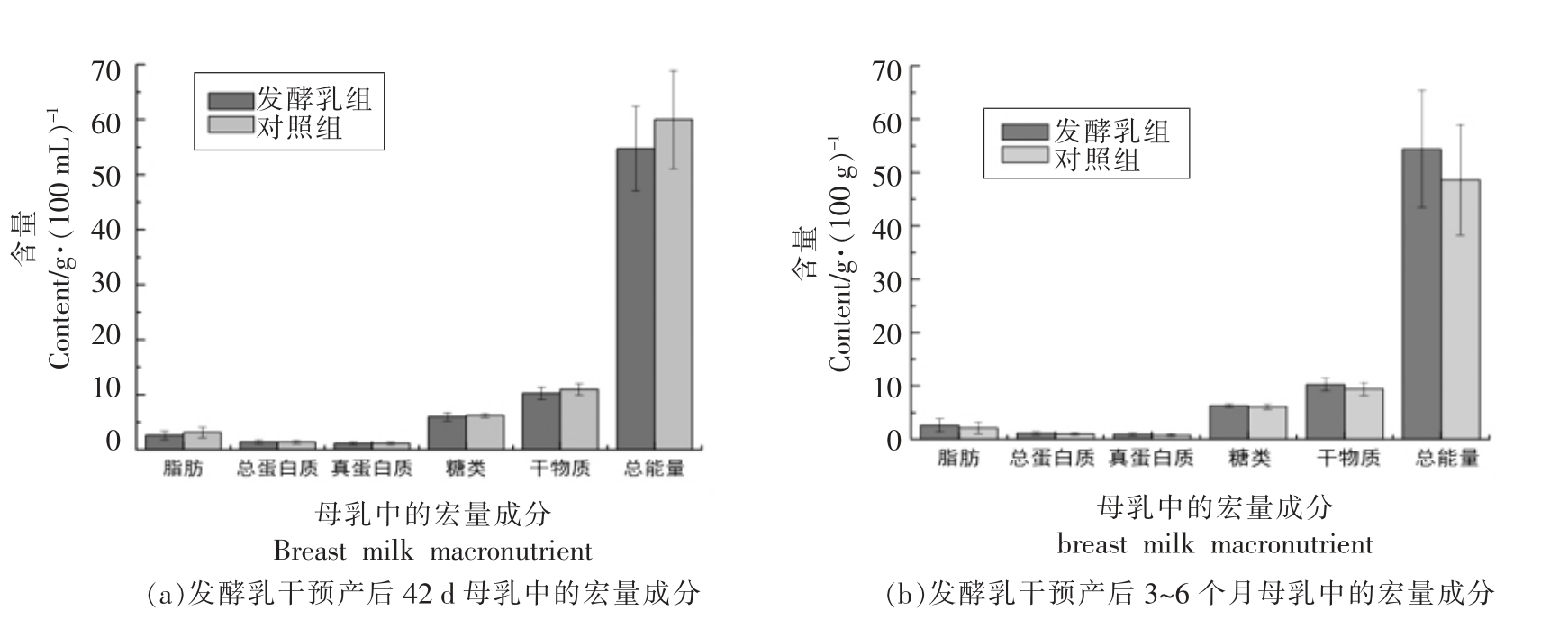
图4 发酵乳干预母乳中的宏量成分
Fig.4 Effect of fermented dairy on breast milk macronutrient
2.5 发酵乳干预对产后母子体重、心理健康及婴幼儿神经发育的影响
根据发酵乳组和对照组在产后1~5 d,产后42 d 以及产后3~6 个月母亲的身体质量指数,发现两组的母亲身体质量指数在产后两个时间点均没有统计学差异(P>0.05)(图5a,5b,5c)。图5d 同样显示在产后1~5 d,产后42 d 以及产后3~6 个月婴幼儿的体重增长在两组中无显著差异 (P>0.05)。

图5 发酵乳干预产后母子身体质量指数和体重
Fig.5 Effect of fermented dairy on mother and child's increased body mass index and weight
发酵乳组和对照组产妇在产后42 d 爱丁堡抑郁量表平均得分分别为5.87 和5.80 分(图6)。发酵乳组有四分之一的人得分超过10 分,有四分之一的人得分低于1.25 分,有一半的人得分是在1.25 和10 分之间;均值高于中位数,说明分值右偏。对照组有四分之一的人得分超过7.4 分,有四分之一的人得分低于2.4 分,有一半的人得分在2.4~7.4 分之间;均值高于中位数,说明分值右偏。发酵乳干预对产后抑郁没有统计学差异。图7显示发酵乳干预对产后42 d 的婴幼儿精细动作仅具有10%水平上的统计学差异,另外发酵乳干预对产后42 d 婴幼儿的沟通、粗大动作、解决问题、个人-社会方面的影响不具有统计学差异。
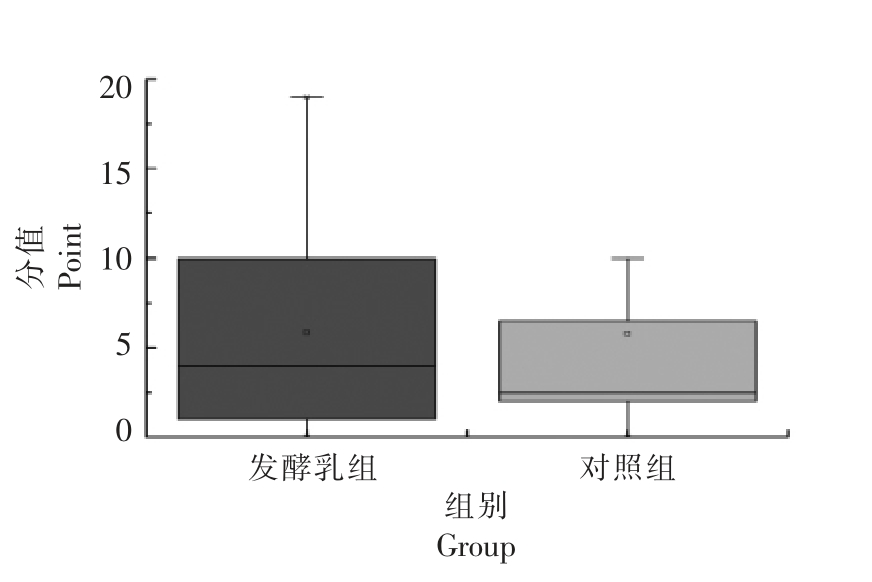
图6 发酵乳干预产后42 d 爱丁堡抑郁量表得分
Fig.6 Effect of fermented dairy on scores of Edinburgh postnatal depression scale during the puerperium
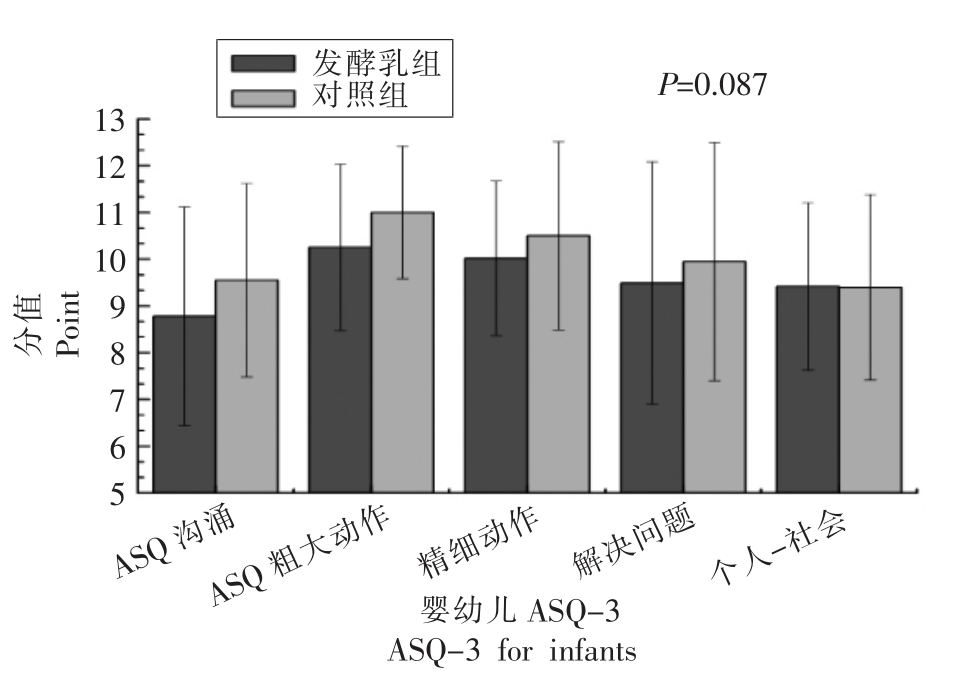
图7 发酵乳干预产后42 d 婴幼儿ASQ-3
Fig.7 Effect of fermented dairy on ASQ-3 for infants during the puerperium
3 讨论
本次临床实验通过检测和解析受试人群产后两个阶段的母乳发现,富含益生菌益生元的发酵乳对母乳微生物的结构具有调节作用。在产后42 d,发酵乳组的痤疮丙酸杆菌、罗斯氏菌、奈瑟氏菌属显著减少,痤疮丙酸杆菌通过表达蛋白酶,使受体、TNF-α、TLR 活化,激活先天性免疫反应以及角质细胞表达IL-8/12/1、基质金属蛋白酶,导致毛囊皮脂腺角化过度[28]。罗斯氏菌可能会导致炎症性肠病的发生[29],奈瑟氏菌属与胰腺癌风险增加有关[30]。另外,不论是在产后42 d,还是产后3~6个月,酸奶组中的链球菌属相对丰度均显著下降,有研究发现链球菌属属于“促癌菌”,该菌可以通过抑制免疫,从而刺激促炎细胞因子的释放,或者直接与癌细胞互作,刺激癌细胞增殖[31]。本项研究表明发酵乳干预对产后3~6 个月的母乳中的真蛋白具有显著促进作用。真蛋白包括α-乳白蛋白、乳铁蛋白、溶菌酶等,α-乳白蛋白具有调节乳糖合成及乳汁分泌的作用[32],乳铁蛋白可抗真菌、抗病毒、抗氧化等[33],溶菌酶具有增强新生儿抗感染能力的作用[34],研究表明真蛋白的合成主要受到乳腺代谢通路的影响,受膳食作用较小。因此,发酵乳干预是否改善了乳腺的代谢通路,以及干预母乳微生物和宏量成分的机制还需进一步研究。本项临床实验研究发现,相较于对照组,发酵乳组在ASQ-3 沟通、粗大动作、解决问题等方面不具有显著差异性,这主要是因为婴儿的神经心理发育受到多种因素的影响。因此,本研究说明富含益生菌益生元的发酵乳通过调整母乳的菌群结构、宏量成分等营养组成,具有提高婴幼儿神经心理发育的潜在作用,具有一定的科学研究价值和前景。
[1]佚名.孕产妇心理健康管理专家共识 (2019年)[J].中国妇幼健康研究,2019,30(7):781-786.
YI M.Consensus on maternal mental health management(2019)[J].Chinese Journal of Woman and Child Health Research,2019,30(7):781-786.
[2]DEWANTO N E,FIRMANSYAH A,SUNGKAR A,et al.The effect of Bifidobacterium animalis lactis HNO19 supplementation among pregnant and lactating women on interleukin-8 level in breast milk and infant's gut mucosal integrity[J].Medical Journal of Indonesia,2017,26(3):204.
[3]ZAIDI A Z,MOORE S E,OKALA S G.Impact of maternal nutritional supplementation during pregnancy and lactation on the infant gut or breastmilk microbiota:A systematic review[J].Nutrients,2021,13(4):1137.
[4]LARA-VILLOSLADA F,OLIVARES M,SIERRA S,et al.Beneficial effects of probiotic bacteria isolated from breast milk[J].British Journal of Nutrition,2007,98(1):96-100.
[5]MARTÍN R,HEILIG G H J,ZOETENDAL E G,et al.Diversity of the Lactobacillus group in breast milk and vagina of healthy women and potential role in the colonization of the infant gut[J].Journal of Applied Microbiology,2007,103 (6):2638-2644.
[6]MAKINO H,KUSHIRO A,ISHIKAWA E,et al.Transmission of intestinal Bifidobacterium longum subsp.longum strains from mother to infant,Determined by multilocus sequencing typing and amplified fragment length polymorphism[J].Applied Environmental Microbiology,2011,77(19):6788-6793.
[7]范玉震,王志忠,裴新颜,等.母乳成分对纯母乳喂养婴幼儿早期生长发育速率的影响[J].中国食物与营养,2020,26(2):78-81.
FAN Y Z,WANG Z Z,PEI X Y,et al.Effects of breast milk composition on early growth and development rates among exclusively breastfed infants[J].Food and Nutrition in China,2020,26(2):78-81.
[8]RIH N,MINOLI I,MORO G.Milk protein intake in the term infant.I.Metabolic responses and effects on growth[J].Acta Paediatrica Scandinavica,2010,75(6):881-886.
[9]吕建利,范煜桢,张健,等.2018年北京市区52 名乳母膳食评价及其与母乳成分的关系[J].卫生研究,2020,49(3):392-396.
LV J L,FAN Y Z,ZHANG J,et al.Dietary evaluation of 52 lactating mothers in Beijing in 2018 and its relationship with breast milk composition[J].Journal of Hygiene Research,2020,49(3):392-396.
[10]余仁强,袁金玲,马路一,等.益生菌对肥胖大鼠血脂紊乱及胰岛素抵抗的影响[J].中国当代儿科杂志,2013,15(12):1123-1127.
YU R Q,YUAN J L,MA L Y,et al.Probiotics improve obesity-associated dyslipidemia and insulin resistance in high-fat diet-fed rats[J].Chinese Journal of Contemporary Pediatrics,2013,15 (12):1123-1127.
[11]PARK S,JI Y,JUNG H Y,et al.Lactobacillus plantarumHAC01 regulates gut microbiota and adipose tissue accumulation in a diet-induced obesity murine model[J].Applied Microbiology & Biotechnology,2017,101(4):1605-1614.
[12]EVERARD A,BELZER C,GEURTS L,et al.Cross-talk between Akkermansia muciniphila and intestinal epithelium controls diet-induced obesity[J].Proceedings of the National Academy of Sciences of the United States of America,2013,110 (22):9066-9071.
[13]SHAO T,TAO H H,NI L L,et al.Maternal prepregnancy body mass index and gestational weight gain with preschool children's overweight and obesity[J].Chinese Journal of Preventive Medicine,2016,50(2):123-128.
[14]GIBSON G R,HUTKINS R,SANDERS M E,et al.Expert consensus document:The International Scientific Association for Probiotics and Prebiotics(ISAPP) consensus statement on the definition and scope of prebiotics[J].Nat Rev Gastroenterol Hepatol,2017,14(8):491-502.
[15]BINDELS L B,DELZENNE N M,CANI P D,et al.Towards a more comprehensive concept for prebiotics[J].Nature Reviews Gastroenterology & Hepatology,2015,12(5):303-310.
[16]ARCHER B J,JOHNSON S K,DEVEREUX H M,et al.Effect of fat replacement by inulin or lupinkernel fibre on sausage patty acceptability,postmeal perceptions of satiety and food intake in men[J].British Journal of Nutrition,2004,91(4):591-599.
[17]TARANTINO G,FINELLI C.Systematic review on intervention with prebiotics/probiotics in patients with obesity-related nonalcoholic fatty liver disease [J].Future Microbiology,2015,10(5):889-902.
[18]NASERIBAFROUEI A,HESTAD K,AVERSHINA E,et al.Correlation between the human fecal microbiota and depression[J].Neurogastroenterology &Motility the Official Journal of the European Gas trointestinal Motility Society,2014,26(8):1155-1162.
[19]LANJEWAR S,NI MK AR S,JUNGARI S.Depressed motherhood:Prevalence and covariates of maternal postpartum depression among urban mothers in India[J].Asian Journal of Psychiatry,2021,57(3):102567.
[20]DAVIS E P,GLYNN L M,SCHETTER C D,et al.Prenatal Exposure to Maternal Depression and Cortisol Influences Infant Temperament[J].Journal of the American Academy of Child & Adolescent Psychiatry,2007,46(6):737-746.
[21]LYONS-RUTH K,CONNELL D B,GRUNEBAUM H U,et al.Infants at social risk:maternal depression and family support services as mediators of infant development and security of attachment[J].Child Dev,2010,61(1):85-98.
[22]MILGROM J,WESTLEY D T,GEMMILL A W.The mediating role of maternal responsiveness in some longer term effects of postnatal depression on infant development[J].Infant Behavior & Development,2004,27(4):443-454.
[23]B L D A,C L G A,D G C A,et al.Effects of the probiotic Bifidobacterium infantis in the maternal separation model of depression[J].Neuroence,2010,170(4):1179-1188.
[24]MESSAOUDI M,LALONDE R,VIOLLE N,et al.Assessment of psychotropic-like properties of a probiotic formulation (Lactobacillus helveticus R0052 and Bifidobacterium longum R0175)in rats and human subjects[J].British Journal of Nutrition,2011,105(5):755-764.
[25]ASMA,KAZEMI,AHMAD,et al.Effect of prebiotic and probiotic supplementation on circulating pro-inflammatory cytokines and urinary cortisol levels in patients with major depressive disorder:A double-blind,placebo-controlled randomized clinical trial-ScienceDirect[J].Journal of Functional Foods,2019,52(1):596-602.
[26]SAVIGNAC H M,CORONA G,MILLS H,et al.Prebiotic feeding elevates central brain derived neurotrophic factor,N-methyl-D-aspartate receptor subunits and D-serine[J].Neurochemistry International,2013,63(8):756-764.
[27]JOHNSTONE S J,BOYCE P M,HICKEY A R,et al.Obstetric risk factors for postnatal depression in urban and rural community samples[J].Australian &New Zealand Journal of Psychiatry,2015,35(1):69-74.
[28]DRÉNO B.What is new in the pathophysiology of acne,an overview[J].Journal of the European Academy of Dermatology and Venereology,2017,31(5):8-12.
[29]LLOYD-PRICE J,ARZE C,ANANTHAKRISHNAN A N,et al.Multi-omics of the gut microbial ecosystem in inflammatory bowel diseases[J].Nature,2019,569(7758):655-662.
[30]JIE C,DOMINGUEB J C,SEARSA C L.Microbiota dysbiosis in select human cancers:Evidence of association and causality [J].Seminars in Immunology,2017,32(8):25.
[31]JAKOPOVI K L,BARUKI I,BOANI R.Physiological significance,structure and isolation of α-lactalbumin[J].Mljekarstvo,2016,66(1):3-11.
[32]LAYMAN D K,BO L,FERNSTROM J D.Applications for α-lactalbumin in human nutrition[J].Nutrition Reviews,2018(6):444-460.
[33]A PERMYAKOV E,E PERMYAKOV S,BREYDO L,et al.Disorder in Milk Proteins:α-Lactalbumin.Part C.Peculiarities of Metal Binding[J].Current Protein and Peptide Science,2016,17(8):735-745.
[34]MINAMI J,ODAMAKI T,HASHIKRUA N,et al.Lysozyme in breast milk is a selection factor for bifidobacterial colonisation in the infant intestine[J].Beneficial Microbe,2016,7(1):53-60.