1 植物蛋白及其结构与柔性化加工
1.1 植物蛋白概述
蛋白质是所有生命活动的物质基础,对人体生理、生化代谢反应起重要的调节作用[1]。在世界人口迅速增长的情况下,植物蛋白作为普遍而又优质的蛋白质资源加以利用,成为一种新的发展趋势。使用不同来源的植物蛋白开发更多安全、营养和美味的食品成为市场的主要发展方向。21世纪被称为植物蛋白世纪,人类对营养高品位和营养均衡的追求日益迫切,主要体现在两个方面:一是发达国家的食品需求趋势正从单纯的动物蛋白向动植物蛋白科学合理搭配这种结构型调整和回归;二是发展中国家和不发达国家正从温饱型向合理营养结构型发展。这两种发展趋势均要求植物蛋白工业给人们提供高品质的植物蛋白产品[2]。
1.2 植物蛋白结构解析
蛋白质分子作为最重要的生物大分子,具有复杂的4 级结构。对蛋白质分子结构学的研究已成为当今科学研究的前沿和热点之一。以大豆蛋白为例,其复杂的分子结构主导了多种功能特性,高度影响蛋白的品质。它是蛋白营养价值、功能特性、储藏加工性质及感官性状等一系列宏观品质形成的决定性因素。根据大豆蛋白质溶解性可以分为大豆清蛋白(albumin,5%左右)和大豆球蛋白(globulin,90%左右)[5]。大豆蛋白质是指贮藏蛋白中的大豆球蛋白(11S,glycinin)和β-伴大豆球蛋白(7S,β-conglycinin),这两种球蛋白含量占大豆总蛋白约70%,且两种球蛋白的功能特性存在显著差异[6-7]。此外,7S 中极性氨基酸含量(53.0%)远远高于11S(28.8%);弱极性氨基酸的总含量相当(7S 为12.1%,11S 为8.7%),而非极性氨基酸总含量则为11S(62.5%)远高于7S(34.8%)[8]。只有系统解决植物蛋白质的结构特性、功能表达规律、构效关系、调控机制等基础科学问题,才能破解目前植物蛋白领域所面临的“卡脖子”现状。
1.3 植物蛋白柔性化加工
蛋白质的空间三维结构是其生化功能及细胞功能的基础,通过蛋白质的三维结构可以了解蛋白质的生物角色、分子间相互作用等重要特征[9]。天然蛋白质结构不是静止不动的,它的随机运动造成蛋白质侧链构象转变,使蛋白质表现出一定的结构柔性,在不同环境条件下,实现其功能的多样性[10]。蛋白质的柔性区间一般可以理解为蛋白质分子中的空间结构中易于发生改变的部分,而结构稳定固化、不易改变的部分称为刚性区间[11]。江连洲团队首次提出大豆蛋白柔性化加工理论的概念,并发现大豆蛋白结构存在柔性区间,且该柔性区间部分影响大豆蛋白结构折叠/解折叠、亚基聚合/解离等,是决定蛋白加工特性及界面功能高效表达的关键[11]。此项研究为植物蛋白产业的整体技术升级和高价值、高品质蛋白产品的开发提供了有力的科技支撑,具有重要的现实意义。
2 植物蛋白加工工艺
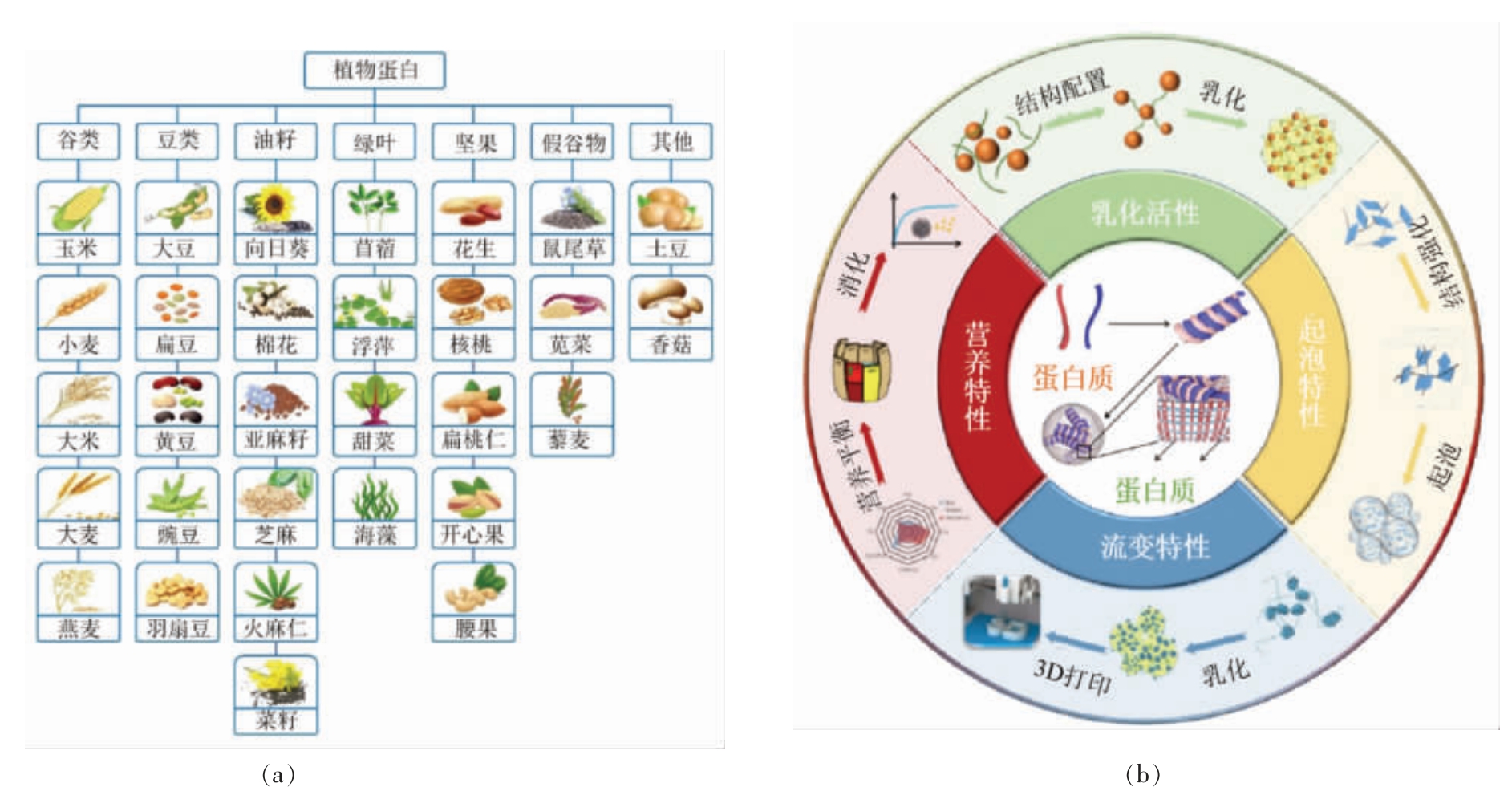
图1 植物蛋白的主要来源及多维应用[3-4]
Fig.1 Main sources and multidimensional applications of vegetable protein[3-4]
植物蛋白具有丰富的营养价值,主要应用于食品体系中。然而,天然植物蛋白因自身结构或加工工艺等因素的影响,功能性质较差,不能满足现代食品工业的需要,需对蛋白质进行适当改性。目前蛋白质改性的工艺有物理改性、化学改性、生物改性及纤维化改性[11]。
2.1 物理加工
物理改性是一种利用热、光、电、声等物理因素改变蛋白质内部结构和分子间作用力的加工方式,具有操作简单、条件温和、安全无污染、对蛋白质营养破坏较小等优点。目前,物理改性处理方法主要包括热处理、电子束辐照、高压均质、超声等[12]。
2.1.1 热处理 热处理是修饰植物蛋白结构和功能特性的常用方法之一。其原理是通过热处理导致蛋白多肽链展开,使蛋白分子内部巯基和疏水侧链暴露,进而影响植物蛋白功能特性。温和的加热条件促进蛋白质展开,增强蛋白功能,极端加热条件会导致蛋白质结构发生不可逆的变化,导致其功能性降低。热处理可以改善植物蛋白的乳化性、发泡性和凝胶特性[20]。除传统加热处理技术外,微波加热[21]、射频加热[22]、红外辐射加热[23]等新型加热技术的研究日益增多。
2.1.2 电子束辐照 电子束辐照技术是一种可控的非热加工过程,具有低成本、高效率等特点,主要应用于食品材料的灭菌以及辅助提取过程。电子束辐照因高能量而影响蛋白质结构中的化学键和分子键,导致蛋白展开和变性,进而改善其功能特性和生物活性[24]。Wang 等[25]发现电子束辐照对小麦胚芽蛋白乳化性、发泡性和抗氧化能力产生积极影响。Li 等[26]发现电子辐照处理后大米蛋白肽的乳化活性从145%提到204%。
2.1.3 高压均质 高压技术是一种操作方便、耗能小、效率高的非热物理加工方法。其主要的作用机制是蛋白在高压(100~800 MPa)条件下通过特定宽度均质区,高压产生的空化效应、高速剪切力和碰撞力使蛋白质均匀分散,形成细小液滴[27]。高压处理使蛋白质的极性和疏水氨基酸暴露,进而改善植物蛋白理化性质和功能性质,如溶解度、持水性、发泡性和乳化性等[28]。高压均质不会影响氨基酸、风味化合物等小分子,几乎不会对蛋白质的营养和感官特性造成影响[29]。
2.1.4 超声波 超声波技术是一种增强蛋白质分散性的新型物理改性技术,具有效率高,加工能耗少,反应条件平和等特点。其作用机理:超声空化过程中产生的剪切力破坏了蛋白质的疏水相互作用或分子间二硫键,导致蛋白质结构改变,影响蛋白的溶解性、乳化性、持水性等功能特性[25]。超声处理在植物蛋白结构修饰和功能特性改善中显示出巨大的应用潜力。
表1 植物蛋白的物理改性方法
Table 1 Physical modification methods of vegetable protein

改性手段 原理 植物蛋白种类 处理条件 提升蛋白理化特性 参考文献热处理热处理诱导蛋白结构部分展开,使分子内部的疏水基团暴露于分子表面,从而增强蛋白分子间相互作用及界面吸附能力大豆蛋白70 ℃,20 min;85 ℃,10 min;85 ℃,20 min;85 ℃,30 min;100 ℃,20 min小麦醇溶蛋白 50,70,90 ℃分别处理15,30,60 min热处理改变SPI 体外消化模式 [13]起泡能力和泡沫稳定性分别提高25%和85% [14]电子束辐照电子束照射(EBI)是电离照射的一种,是通过电的加速和转换产生的。电子在接触暴露的样品时会改变各种化学键和分子键,自由基可能通过电离产生大米蛋白 5,10,25,50,75 kGy,照射5.0 MeV乳化活性和稳定性分别比未辐照样品提高145%和204%[15]高压均质利用湍流、高速剪切等作用力,诱导蛋白化学键的形成与破坏,影响蛋白分子间的相互作用,从而提升蛋白各项理化特性大豆蛋白 0,30,60,90,120 MPa 乳化活性和乳化稳定性增加 [16]大米蛋白 0,5,40,80,120 MPa溶解性和乳化活性均有所提高,分别在120 MPa 和80 MPa 达到最大[17]超声利用超声波产生的空化效应,促使蛋白分子展开和部分变性,内部活性基团暴露,从而改善植物蛋白各项理化特性葵花籽蛋白 100,300,500,700 W分别处理30 min超声功率为700 W 时葵花籽蛋白的溶解性、乳化性和起泡性分别提高21.18%,1.87 m2/g 和11.03%花生蛋白超声功率500 W,处理时间分别为10,20,30,40 min超声时间为20 min 时,PPIMP 具有最小的粒径,最大的表面疏水性、乳化性和乳化稳定性[18][19]
2.2 化学加工
化学改性是一种通过化学反应改变蛋白质的理化功能性质的改性方法之一。常见的蛋白质化学改性方法包括糖基化、磷酸化、酰化、去酰胺、pH 改性等。化学改性具有效率高,成本低,操作简单等优点。然而,该技术使用化学品并产生化学副产品,对食品安全性和营养方面有不利影响[30]。
2.2.1 糖基化 目前制备蛋白质-多糖络合物的方法主要有干热法、湿热法。干热法是指通过控制温度、湿度和糖化时间对固体反应底物进行加热[37]。然而,干热法具有反应周期长,成本高,难以大规模生产等缺点。湿热法可弥补这一缺陷,该方法是将蛋白和多糖在溶液中进行加热反应。大多数研究表明,由于糖基化后蛋白形成更厚的界面层,更大空间位阻和/或静电斥力,植物蛋白在与不同糖类缀合后乳化性能得到改善[38]。
2.2.2 磷酸化 磷酸化是一种将磷酸基团引入蛋白质初级序列中,在很大程度上调节其功能的化学改性手段。植物性蛋白质的功能性质在磷酸化后得到改善,且该反应对蛋白消化无显著影响,是一种较实用、有效的改性方法[39]。磷酸化修饰植物蛋白依赖于pH 值、温度和磷酸盐浓度,在较高的pH 值、温度和磷酸盐浓度下可以实现更高程度的磷酸化[40]。
2.2.3 酰化 酞化反应是酰化试剂与氨基酸中的亲核基团发生反应,该过程可根据所使用的酰化剂乙酸或琥珀酸酐分为乙酰化和琥珀酰化。酰化可以改变植物蛋白的二级和三级结构,有效提高溶解度等功能特性,而不会对其营养产生不利影响。目前,酰化对植物蛋白的影响研究包括燕麦、小麦、大豆、豌豆、葵花籽、花生和叶蛋白等[41]。
表2 植物蛋白的化学改性方法
Table 2 Chemical modification method of vegetable protein
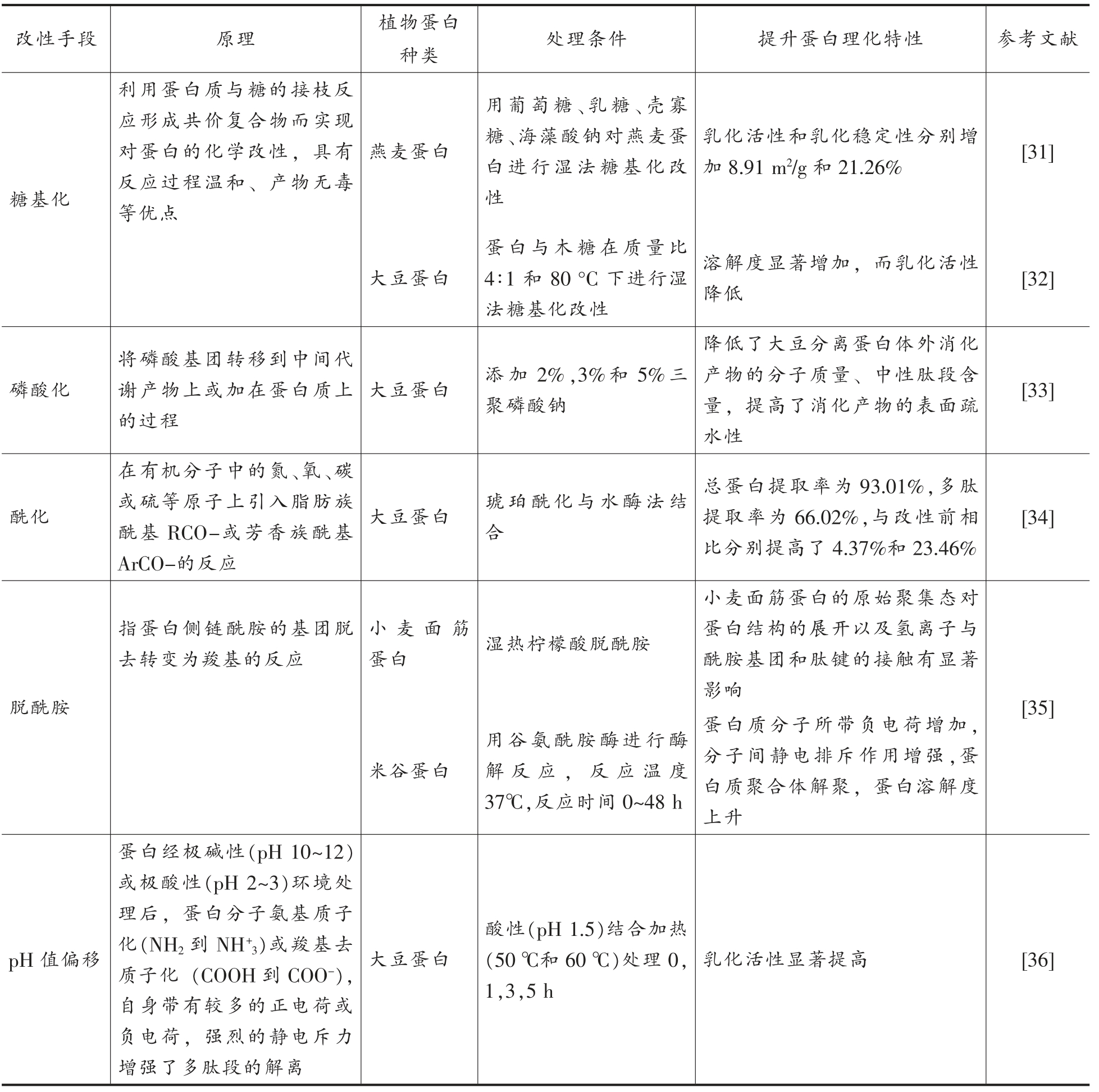
改性手段 原理 植物蛋白种类 处理条件 提升蛋白理化特性 参考文献糖基化利用蛋白质与糖的接枝反应形成共价复合物而实现对蛋白的化学改性,具有反应过程温和、产物无毒等优点燕麦蛋白用葡萄糖、乳糖、壳寡糖、海藻酸钠对燕麦蛋白进行湿法糖基化改性乳化活性和乳化稳定性分别增加8.91 m2/g 和21.26% [31]大豆蛋白蛋白与木糖在质量比4∶1 和80 °C 下进行湿法糖基化改性溶解度显著增加,而乳化活性降低 [32]磷酸化酰化将磷酸基团转移到中间代谢产物上或加在蛋白质上的过程在有机分子中的氮、氧、碳或硫等原子上引入脂肪族酰基RCO-或芳香族酰基ArCO-的反应大豆蛋白 添加2%,3%和5%三聚磷酸钠大豆蛋白 琥珀酰化与水酶法结合降低了大豆分离蛋白体外消化产物的分子质量、中性肽段含量,提高了消化产物的表面疏水性总蛋白提取率为93.01%,多肽提取率为66.02%,与改性前相比分别提高了4.37%和23.46%[33][34]脱酰胺指蛋白侧链酰胺的基团脱去转变为羧基的反应小麦面筋蛋白 湿热柠檬酸脱酰胺米谷蛋白用谷氨酰胺酶进行酶解反应,反应温度37℃,反应时间0~48 h小麦面筋蛋白的原始聚集态对蛋白结构的展开以及氢离子与酰胺基团和肽键的接触有显著影响 [35]蛋白质分子所带负电荷增加,分子间静电排斥作用增强,蛋白质聚合体解聚,蛋白溶解度上升pH 值偏移蛋白经极碱性(pH 10~12)或极酸性(pH 2~3)环境处理后,蛋白分子氨基质子化(NH2 到NH+3)或羧基去质子化(COOH 到COO-),自身带有较多的正电荷或负电荷,强烈的静电斥力增强了多肽段的解离大豆蛋白酸性(pH 1.5)结合加热(50 ℃和60 ℃)处理0,1,3,5 h乳化活性显著提高 [36]
2.2.4 脱酰胺 脱酰胺是将谷氨酰胺基团和天冬酰胺残基转化为蛋白质内的羧基,增强蛋白质的负电荷的化学改性方法。该方法条件温和,无需添加额外分子,是一种蛋白质的安全修饰方法。He等[42]使用乙酸、酒石酸和柠檬酸的酸性脱酰胺来掩盖小麦面筋水解物的苦味。Jiang 等[43]利用谷氨酰胺酶脱酰胺改性燕麦蛋白,显示出较好的溶解度和乳化特性。Kunarayakul 等[44]观察到谷氨酰胺酶脱酰胺后,椰子蛋白的溶解度、乳化和发泡特性得到改善。
2.2.5 pH 值偏移 酸性或碱性处理会引发蛋白质结构和功能性质的变化。在极端pH 值条件下,蛋白质变性并展开,暴露出巯基和疏水基团,这导致其分子和二级结构的变化,改善其功能特性[45]。Lee 等[15]改变蛋白质pH 值为12,然后,超声处理制备纳米级大豆蛋白聚集体,其溶解度、表面疏水性和乳化能力显著增强。通过碱和超声联合处理植物蛋白,其溶解度、乳化性和发泡性能也得到改善[46]。
2.3 生物加工
酶解和发酵是一种通行的生物改性技术,具有环境友好、能耗低、无毒副产品等特点。除了调节蛋白质功能外,这些方法还具有改善其消化率、生物利用度以及抗氧化和抗菌特性等能力。酶法改性分为酶水解法和酶交联法,是改变结构的蛋白质修饰方法之一。因作用机制不同,故不同的酶具有不同的最终产品性质和功能。Eckert 等[47]观察到胃蛋白酶水解后蚕豆蛋白的发泡性和持油性显著提高。发酵是一种用于植物蛋白修饰的生物改性方法,不同的发酵剂被应用于发酵植物蛋白,如乳酸菌、酵母菌、霉菌和芽孢杆菌等。目前,多项研究表明发酵可改善植物蛋白溶解度、持水性和发泡性[48-49]。发酵不仅影响植物蛋白的结构和功能特性,还促进其营养特性和生物活性提高。Yang 等[50]发现花生蛋白发酵后,其消化率显著增加。发酵还可通过降解植物蛋白的过敏原和抗营养成分来降低其致敏性[51]。
2.4 淀粉样蛋白纤维化
淀粉样蛋白纤维化是通过各种途径制备的纤维状蛋白聚集体。其方法是将蛋白在酸性条件下加热,使其水解并展开,最终自组装形成淀粉样蛋白聚集体[52]。由于蛋白质原纤维具有高纵横比和有序结构等结构特点,包括更稳定的物理性质、黏度、发泡性能和乳化活性,以及出色的生物活性,包括抗氧化性、抗菌活性和低致敏性,扩大了它们在功能性胶体分散中的潜力[53]。目前,淀粉样蛋白纤维化主要应用于动物蛋白,特别是乳清蛋白,而在植物蛋白中的应用较少。pH 值对大豆分离蛋白淀粉原纤维形成有影响,在不同的pH 值下,原纤维具有不同形状[54]。Tong 等[55]研究了超声预处理对大豆蛋白原纤维的影响,发现超声辅助EGCG处理的大豆蛋白原纤维具有较好的稳定性、黏度和抗氧化活性。虽然植物蛋白的纤维化是一种非常有效、新颖的改性方法,但是淀粉样纤维具有一定的安全隐患。
3 植物蛋白的应用
植物蛋白已广泛应用于食品工业各领域,如:用作食品成分、补充剂、乳化剂、功能水解物、可食用涂层成分以及各种功能化合物的载体,具体表现为植物蛋白肉、植物蛋白奶、植物蛋、植物蛋白肽以及植物蛋白薄膜等。
3.1 植物蛋白肉
植物蛋白肉即组织化植物蛋白,是人造肉的一种。一般而言,采用低水分挤压技术制造的产品具有干燥和轻微膨胀的特点,由于设备成本低且技术成熟,因此仍是目前应用广泛的加工技术[56]。而高水分挤压新型植物肉加工技术,一般要求物料的蛋白质含量达到60%以上,且被挤压物料的含水量在40%~80%,可生产含水量高、无需再水化、弹性强、营养成分损失少且纤维结构更接近真实肉类的产品,从而避免了在低水分条件下咀嚼产品时出现的口感和质地差的问题。
进一步研究需侧重优化技术参数,改善营养和安全,丰富产品口味,以满足消费者对产品质量的需求;各技术参数以及蛋白质来源对原料间的相互作用,各向异性纤维结构的形成以及最终产品的质量都有很大的影响,并且非蛋白质成分对于植物蛋白肉的生产也至关重要[57]。
在大多数情况下,挤出物的各向异性程度是挤出质量的最重要指标之一,也是影响消费者接受度的关键因素[58]。Do Carmo 等[59]使用高水分挤压从蚕豆浓缩蛋白生产植物蛋白肉,在130~140 ℃温度范围,水与产品进料速率之比为4,进料速率为11 r/min(1.10 kg/h)下生产的植物蛋白肉具有最好的感官和质地特性,符合该产品类别相关的属性。Dou 等[60]比较3 种食品胶对大豆蛋白高水分挤压蒸煮法制备的挤压物品质的影响,并确定负责形成挤出物的分子键类型的重要性排序为:二硫键≥氢键相互作用>疏水相互作用。此外,该团队以大豆浓缩蛋白为原料,添加不同比例海藻酸钠,改变模头温度,采用双螺杆高水分挤压技术制备植物肉,结果表明:海藻酸钠添加量6%时,可制备组织化程度高,蒸煮效果较好的大豆浓缩蛋白挤压植物肉产品[61]。Zhang 等[62]研究大豆蛋白和小麦面筋混合物的高水分挤压过程中纤维结构形成的潜在机制,结果表明:氢键和二硫键在挤出过程中起主要作用,二硫键从分子内模式转变为分子间模式,蛋白α-螺旋向β-折叠的转变,保持理想的平衡,这对于纤维结构的形成至关重要。
虽然植物蛋白肉的研究取得初步成功,但是其大规模工业化应用仍面临挑战,除模仿肉类质地和风味的技术障碍外,食品安全和营养也存在其它尚未充分解决的潜在障碍[63]。例如:必须对添加的虽广泛可用但易过敏的植物蛋白质,各种其它成分与添加剂,以及可能的微生物污染进行系统地考查研究。
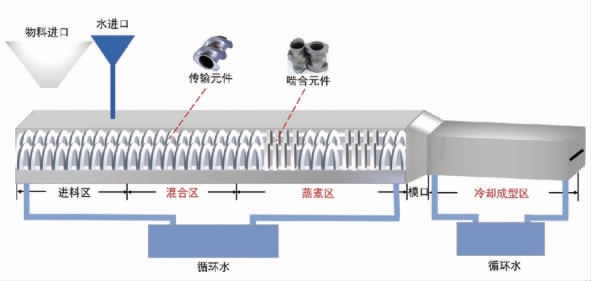
图2 高水分挤压功能区示意图[64]
Fig.2 Schematic diagram of the high moisture extrusion functional area[64]
表3 大豆蛋白肉类似物的加工参数和特性
Table 3 Processing parameters and characteristics of soy protein meat analogs
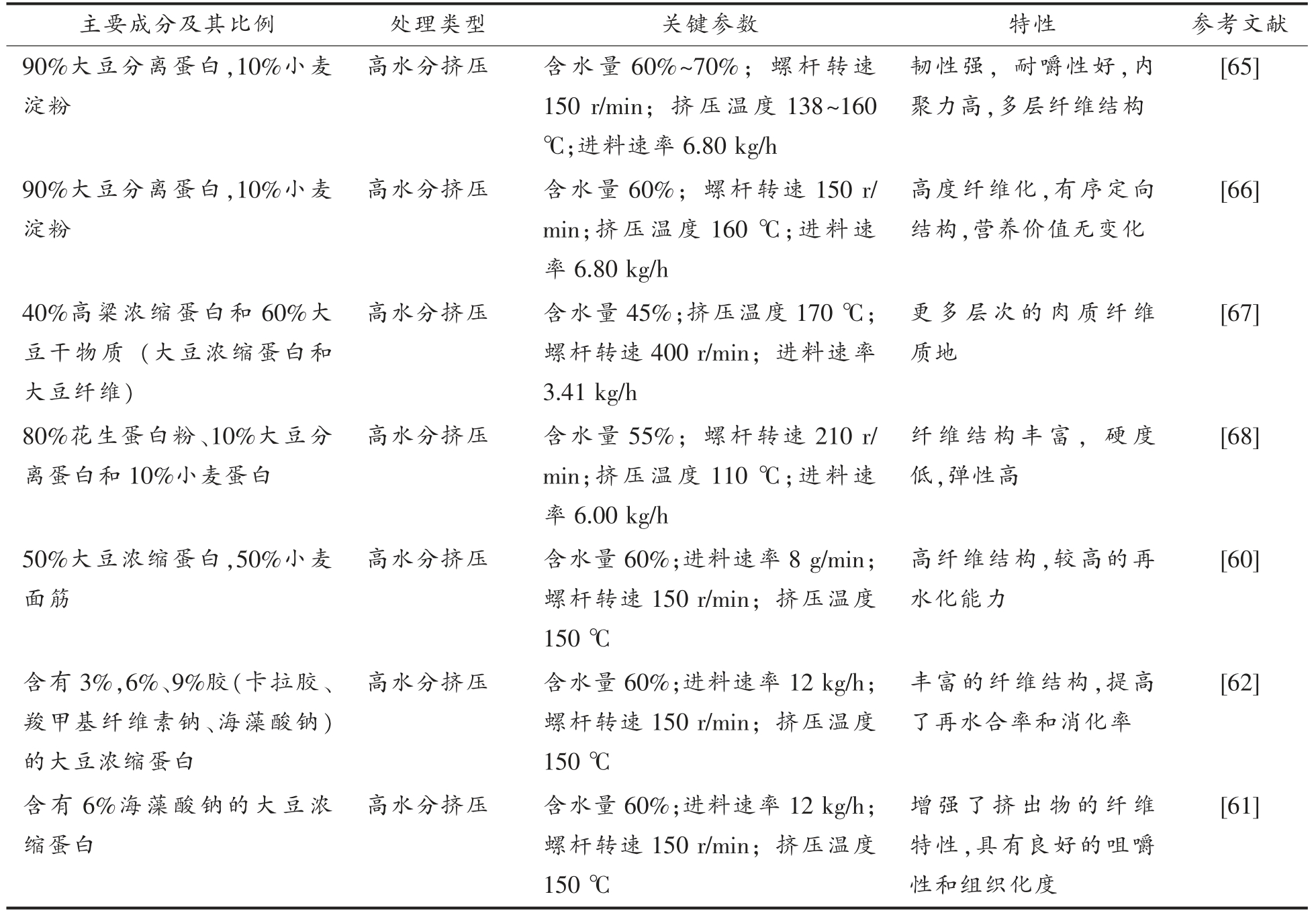
主要成分及其比例 处理类型 关键参数 特性 参考文献90%大豆分离蛋白,10%小麦淀粉高水分挤压 含水量60%~70%;螺杆转速150 r/min;挤压温度138~160℃;进料速率6.80 kg/h韧性强,耐嚼性好,内聚力高,多层纤维结构[65]90%大豆分离蛋白,10%小麦淀粉40%高粱浓缩蛋白和60%大豆干物质(大豆浓缩蛋白和大豆纤维)80%花生蛋白粉、10%大豆分离蛋白和10%小麦蛋白50%大豆浓缩蛋白,50%小麦面筋含有3%,6%、9%胶(卡拉胶、羧甲基纤维素钠、海藻酸钠)的大豆浓缩蛋白含有6%海藻酸钠的大豆浓缩蛋白高水分挤压 含水量60%;螺杆转速150 r/min;挤压温度160 ℃;进料速率6.80 kg/h高水分挤压 含水量45%;挤压温度170 ℃;螺杆转速400 r/min;进料速率3.41 kg/h高水分挤压 含水量55%;螺杆转速210 r/min;挤压温度110 ℃;进料速率6.00 kg/h高水分挤压 含水量60%;进料速率8 g/min;螺杆转速150 r/min;挤压温度150 ℃高水分挤压 含水量60%;进料速率12 kg/h;螺杆转速150 r/min;挤压温度150 ℃高水分挤压 含水量60%;进料速率12 kg/h;螺杆转速150 r/min;挤压温度150 ℃高度纤维化,有序定向结构,营养价值无变化更多层次的肉质纤维质地纤维结构丰富,硬度低,弹性高高纤维结构,较高的再水化能力丰富的纤维结构,提高了再水合率和消化率增强了挤出物的纤维特性,具有良好的咀嚼性和组织化度[66][67][68][60][62][61]
3.2 植物蛋白奶
越来越多的消费者出于健康原因(如牛奶蛋白过敏、乳糖不耐受)或是对植物性食物的偏好选择植物蛋白奶,这使全球市场的份额不断增长并发展迅速。植物蛋白奶一般是通过在水中提取原材料、分离液体和配制最终产品来制造的,而采用均质和热处理工艺对于提高最终产品的悬浮性和微生物稳定性是必不可少的[69]。目前正在研究一些新的非热加工技术,如高压均质与超声波加工,以解决在不使用高温的情况下延长保质期以及乳液稳定性、营养完整性和感官可接受性等问题。
Bernat 等[70]研究表明,均质化过程虽会减小杏仁和榛子饮料中的粒径,但产生的乳液不稳定,发生相分离。而当将低热处理(85 ℃/30 min)与均质化过程相结合时,两种饮料储存期间的物理稳定性和外观都得到改善,这是因为在热处理期间蛋白质溶解与随后变性的关联,有助于稳定颗粒分散,避免相分离。Salve 等[71]对新鲜提取的花生奶进行不同强度(200,300 W 和400 W,20 kHz)的超声处理以提高质量,这是因为在高能量密度和持续时间条件下可以提高微生物灭活能力,还可以破坏花生细胞,增加植物蛋白奶中水解蛋白质含量,得到更好的沉降指数以避免相分离,并通过更小的颗粒和脂肪球尺寸来改善微观结构。
植物蛋白奶的出现为消费者提供了多样化的营养选择。作为新兴产业的一员,目前植物蛋白奶仍存在一些阻碍发展的瓶颈问题,例如存在抗营养因子以及产品品类单一化等。鉴于此,采用先进的加工技术来提高植物蛋白奶品质尤为重要。
表4 创新技术对植物基非乳制品替代牛奶的影响
Table 4 Impact of innovative technologies on plant-based non-dairy alternative milk

创新技术 植物基质 工艺条件 特性 参考文献超声处理 杏仁 300 W/100%/20 kHz/ 0~5 min 加工时间的延长提高了产品的可溶性固形物含量和物理稳定性,降低其黏度和悬浮颗粒大小[72]超声处理 杏仁 20 kHz/1,4,8,12,16 min 增加体外蛋白质消化率,增加加工时间 [73]高压处理 大豆 200,300 MPa/55,65,75 ℃ 压力和温度的升高促进了豆浆中植物甾醇和异黄酮含量升高,而生育酚含量降低[74]高压处理 大豆 200,300 MPa/55,65,75 ℃ 压力升高促进了更有效的酶失活,在300 MPa和75 ℃下处理可使产品完全灭菌微波 大豆 2.45 GHz/ 70,85,100 ℃/2,5,8 min温度升高和加工时间增加提高了消化率,消除了抗营养因子(胰蛋白酶)[75][76]欧姆加热 大豆 50,500,5 000 Hz,10 kHz/160,180,200,220 V/0,1,3,5,10,15 min/90 ℃频率增加促进了脲酶的高度失活 [77]
3.3 植物蛋
植物蛋是一种由大豆、高粱、豌豆等植物蛋白适当混合调配而成的粉末状食品,具有高营养,低胆固醇等特点,其营养价值高且绿色安全,可用于多种食品的烹调,如炒蛋、甜点烘焙、制作蛋黄酱等[78]。以植物为基础的植物蛋提供了一种非动物源,健康、环保的传统鸡蛋替代品。
与人造鸡蛋不同,植物蛋不追求外形的逼真,而是模拟真鸡蛋的理化和功能属性。为了达到真鸡蛋在烹饪条件下经历的凝胶转变,植物蛋通常需要更高的温度和更长的加热时间才能形成与真鸡蛋类似的结构和纹理,这些性质通常取决于蛋白质类型、浓度与环境条件[79]。目前,已有研究利用绿豆蛋白和乳化菜籽油生产植物蛋[80]。此外,植物蛋因植物基成分表现出良好的乳化性能而被应用于蛋黄酱等调味品中。
3.4 植物蛋白肽
植物蛋白是生物活性肽生产中动物源蛋白的良好替代品。目前,多肽的制备方法主要有化学萃取、发酵、合成和酶水解。化学萃取技术成熟且应用广泛,然而,化学试剂消耗量大、设备成本高,易引起环境污染;发酵方法制备的肽产量高、口感好且成本低,然而,发酵时间较长,易受微生物感染而引发安全问题[81]。合成方法制备的多肽纯度与成熟度高,然而,方法成本高、收率低[82]。相比之下,酶水解方法反应控制简单、重复性好、成本低且能耗低,更适合工业化生产,然而,存在酶解时间长、效率低以及酶对肽纯度有影响等缺点[83]。例如:Suetsuna 等[84]用胃蛋白酶水解小麦面筋蛋白,获得的两种肽(Leu-Gln-Pro-Gly-Gln-Gln-Gln-Gln-Gln-Gly 和Ala-Gln-Ile-Pro-Gln-Gln-Gln-Gln)具有良好的抗氧化能力。Zhu 等[85]研究表明,用碱性蛋白酶水解小麦胚蛋白,其产物具有良好的自由基清除能力。目前已从豆类蛋白质中鉴定出许多抗真菌肽,并对其进行抗植物和人类病原体等试验[86]。在Freitas 等[87]的一项研究中,从豆粕蛋白中分离出12 种生物活性肽,它们对革兰氏阳性和革兰氏阴性食源性病原体的生长有抑制作用,体外毒理学试验表明,大豆抗菌肽对成纤维细胞和小鼠骨髓均无毒性。Puchalska 等[88]研究大豆肽VLIVP 是通过蛋白酶P 从大豆蛋白水解物中分离出来的,与牛奶肽IPP 和VPP 相比,它具有更高的ACE 抑制活性。Yu 等[89]发现用碱性蛋白酶水解花生粉获得的水解产物具有良好的ACE 抑制活性,其小于5 ku 的肽组分比粗水解产物具有更高的ACE 抑制活性。此外,Wen 等[90]从大豆蛋白水解物中鉴定出51 个肽,其中46 个肽被指定为免疫调节肽。他们发现,大豆免疫调节肽可在mRNA 水平上调节包括TNF-α 和IL-6 在内的细胞因子的功能,促进巨噬细胞的增殖,并提高免疫系统介质NO 的水平。
目前虽有许多研究声称植物源性蛋白肽对健康有益,但仍需更深入的研究,如体内消化与代谢,肽发挥生物活性的途径及其作用机制等。在大规模工业化生产时,纯化是生产植物源性生物活性肽的关键步骤。
3.5 植物蛋白薄膜
植物蛋白具有良好的机械和功能特性(良好的生物降解性、可再生性和生物相容性),在生物降解包装系统中具有巨大的应用潜力,可作为传统合成聚合物的新兴替代品[91]。植物蛋白可食用薄膜具有良好的机械性能,对气体(氧气和二氧化碳)的阻隔性能出色,可保护食品免受水分和香气损失[92]。由于可用性和成本较低,植物来源比动物来源的蛋白质在制备薄膜时更常用,并可以通过各种物理、化学和酶法来增强基于蛋白质的膜的性能,以提高效率[93]。
Erdem 等[94]以大豆分离蛋白和葵花籽油为原料,开发了一种基于冷冻干燥的新型生物复合可食用膜生产方法,该膜具有更高的拉伸强度,即更强的膜结构。Cheng 等[95]研究了高强度超声处理对豌豆蛋白薄膜结构和性能的影响,通过超声波改变蛋白质的二级和三级结构,使其具有更好的透明度、拉伸强度和阻水性能,以达到改善蛋白薄膜性能的目的。同时,该团队还将高压均质应用于豌豆蛋白的结构改性,并成功利用这种结构改性来形成性能更好的可食用膜[96]。Zhang 等[97]研究了菜籽蛋白水解物对壳聚糖膜抗菌性能的影响,与壳聚糖膜相比,添加蛋白质水解物的复合膜的抗菌活性更高。
目前作为屏障的可生物降解包装材料的主要局限性在于其渗透性,这值得关注和深入研究,使其不渗透水蒸气、气体和一些有机分子。此外,大规模经济生产植物蛋白基生物可降解材料仍是一个挑战,尤其是在加工方面的困难还需更多的研究[98]。
4 存在问题
植物蛋白作为优质的蛋白资源,具有很好的开发潜能。因为它们比动物蛋白更具优势,特别是在可持续性和动物福利方面。然而,植物蛋白功能性较差,加工过程中功能特性易受影响,部分具有异味等。这些问题限制了植物蛋白在食品、医疗、材料等方面的应用。针对上述问题,许多研究学者进行深入研究并取得喜人的成果。然而,目前我国植物蛋白加工业还存在一些亟待解决的问题:
1)由于植物蛋白的结构多样性和复杂性,加工技术与蛋白质的高阶结构和性质之间的关系仍未确立。
2)目前对植物蛋白的加工改性研究主要集中在实验室规模上。虽有一些中试规模的研究,但改性加工工艺放大到工业规模仍需系统研究。
3)植物蛋白精深加工技术共性装备与个性设备的衔接不配套,植物蛋白制品生产工艺与装备的结合尚不够完美。
4)缺乏创新性核心加工技术。植物蛋白及其产品同质化现象严重,产品种类单一、质量稳定性差、特色及功能性差,无法满足食品加工多领域的需求。此外,国际各大公司实施严密的技术封锁,中国企业无法通过引进、合作等方式获得其核心技术。只有依靠自主科技创新,研制出完全拥有自主知识产权的植物蛋白和植物蛋白基食品加工关键科学技术,才能摆脱国外的技术和产品垄断。
5 未来展望
食品行业正在积极寻找替代蛋白质的新来源,其部分原因是消费者对蛋白质的需求增加,以及过度食用肉类对健康的担忧和对环境的影响。植物蛋白在自然界中具有难以置信的巨大可用性,包括快速生产、广泛可及、高可持续性、绿色制造等。鉴于对低碳、环保和更健康饮食的严格要求,目前正在强调植物蛋白作为动物肉、动物奶等在食品中多维应用的潜在补充物。传统的植物蛋白来源,如大豆、小麦、高粱等正在被再次作为健康和可持续的解决方案来应对这种不断增长的蛋白质需求。目前大豆在植物蛋白方面继续占据主导地位,而基于谷物、其它豆类和坚果的一系列新产品也开始涌现。
关于植物蛋白领域的研究可概括为两种基本策略,即:蛋白质强化和互补。蛋白质互补策略被用于混合缺乏必需氨基酸的食品和提供限制性氨基酸的其它产品的各种组合中。许多植物源,如大豆、小麦、水稻、高粱、玉米、芝麻和亚麻籽,被用于分离高质量蛋白质,并进一步用于补充食物。鉴于植物蛋白的功能特性,其被用作稳定剂、乳化剂、结构剂和食品质地改良剂,用于开发纯素和素食食品,并通过物理、化学、酶法与联合加工过程对蛋白质的功能和感官特性进行修改。
未来,植物蛋白可在满足食品蛋白需求方面发挥更重要的作用,同时有助于增强粮食安全和可持续环境。从环境可持续性和粮食安全的角度来看,迫切需要增加植物蛋白在人类食品中的直接使用,并通过各种加工过程对蛋白质的功能与感官特性进行修改。虽然植物蛋白的各种加工技术已取得很大的成就,但是仍有待开发完全有效的加工方法,使加工过程精准化、高效化,以便充分开发利用具有高营养价值与功能特性的蛋白质,进而加快推进植物蛋白的深度产业化应用。
[1]WU G,FANZO J,MILLER D D,et al.Production and supply of high-quality food protein for human consumption:sustainability,challenges,and innovations[M].Annals Reports,2014,1321(1):1-19.
[2]江连洲.植物蛋白工艺学[M]// 植物蛋白工艺学.北京:科学出版社,2011:1-7.
JIANG L Z.Plant protein technology[M]// Plant Protein Technology.Beijing:Science Press,2011:1-7.
[3]HADIDI M,JAFARZADEH S,FOROUGH M,et al.Plant protein-based food packaging films;recent advances in fabrication,characterization,and applications[J].Trends In Food Science & Technology,2022,120(2):154-173.
[4]KUMAR M,TOMAR M,POTKULE J,et al.Functional characterization of plant-based protein to determine its quality for food applications[J].Food Hydrocolloids,2022,123(2):106986.
[5]DERBYSHIRE E,WRIGHT D J,BOULTER D.Legumin and vicilin,storage proteins of legume seeds[J].Phytochemistry,1976,15(1):3-24.
[6]KITAMURA K.Breeding trials for improving the food-processing quality of soybeans[J].Trends Food Sci Technol,1993,4(3):64-67.
[7]YAGASAKI K,TAKAGI T,SAKAI M,et al.Biochemical characterization of soybean protein consisting of different subunits of glycinin[J].Journal of Agricultural Food Chemistry,1997,45(3):656-660.
[8]RIBLETT A L,HERALD T J,SCHMIDt K A,et al.Characterization of beta-conglycinin and glycinin soy protein fractions from four selected soybean genotypes[J].Journal of Agricultural Food Chemistry,2001,49(10):4983-4989.
[9]SCHLESSINGER A,ROST B.Protein flexibility and rigidity predicted from sequence[J].Proteins-structure Function & Bioinformatics,2005,61(1):115-126.
[10]刘佳,张可辉,罗巧,等.蛋白质柔性区间的预测方法研究进展[J].药物生物技术,2009,16(6):578-581.
LIU J,ZHANG K H,LUO Q,et al.Research progress on prediction methods of protein flexibility interval[J].Pharmaceutical Biotechnology,2009,16(6):578-581.
[11]江连洲,朱颖,王中江.大豆蛋白结构柔性与界面功能的构效关系[J].中国食品学报,2020,20(1):6.
JIANG L Z,ZHU Y,WANG Z J.Structure-activity relationship between structural flexibility and interface function of soybean protein[J].Journal of Chinese Institute of Food Science and Technology,2020,20(1):6.
[12]LIU J,RU Q,DING Y.Glycation a promising method for food protein modification:Physicochemical properties and structure,a review[J].Food Research International,2012,49(1):170-183.
[13]赵城彬,尹欢欢,鄢健楠,等.不同热处理条件下大豆蛋白体外模拟消化产物结构和分子质量分布[J].中国食品学报,2020,20(5):7.
ZHAO C B,YIN H H,YAN J N,et al.Structure and molecular weight distribution of soybean protein simulated digestion products in vitro under different heat treatment conditions[J].Journal of Chinese Institute of Food Science and Technology,2020,20(5):7.
[14]王立峰,朱洁,熊文飞,等.热效应对小麦醇溶蛋白起泡性与结构的影响[J].中国农业科学,2021,54(4):820-830.
WANG L F,ZHU J,XIONG W F,et al.Effects of thermal effects on the foamability and structure of wheat gliadin[J].China Agricultural Science,2021,54(4):820-830.
[15]LEE H,YILDIZ G,DOS SANTOS L C,et al.Soy protein nano -aggregates with improved functional properties prepared by sequential pH treatment and ultrasonication[J].Food Hydrocolloids,2016,55(4):200-209.
[16]郭增旺,郭亚男,李柏良,等.高压均质条件下大豆蛋白热聚集体结构和乳化特性研究[J].农业机械学报,2021,52(4):351-358,74.
GUO Z W,GUO Y N,LI B L,et al.Study on the structure and emulsifying properties of soybean protein thermal aggregates under high pressure homogenization[J].Chinese Journal of Agricultural Machinery,2021,52(4):351-358,74.
[17]张晶,丁芳,邹晴晴,等.高压均质对大米蛋白功能特性及物化特性的影响[J].食品与机械,2016,32(6):9-12,33.
ZHANG J,DING F,ZOU Q Q,et al.Effects of high pressure homogenization on functional and physicochemical properties of rice protein[J].Food and Machinery,2016,32(6):9-12,33.
[18]邓爱华,汤须崇,王云,等.超声波对葵花籽蛋白功能特性的影响[J].食品科技,2022,47(2):90-94.
DENG A H,TANG X C,WANG Y,et al.Effect of ultrasound on the functional properties of sunflower seed protein[J].Food Science and Technology,2022,47(2):90-94.
[19]葛艳争,石爱民,任广跃,等.超声预处理对花生分离蛋白微凝胶颗粒结构及其Pickering 乳液特性的影响[J/OL].食品科学,(2021-12-21)[2022-06-01].https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CAPJ&dbname=CAPJLAST&filename=SPKX202112 1701F&uniplatform=NZKPT&v=3RAbDEYpQvkBpjf8 WYixOSXmP8KDUhxcC6c1Vs5Avzq35275E0uCLByl2R IJ-tpY.
GE Y Z,SHI A M,REN G Y,et al.Effects of ultrasonic pretreatment on the particle structure of peanut protein isolate microgels and the properties of Pickering emulsions[J/OL].Food Science,(2021-12-21)[2022-06-01].https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CAPJ&dbname=CAPJLAST&filename=SPKX2021121701F&uniplatform=NZKPT&v=3RAbDEYpQvkBpjf8WYixOSXmP8KDUhxcC6c1Vs5Av zq35275E0uCLByl2RIJ-tpY.
[20]PEYRANO F,SPERONI F,AVANZA M V.Physicochemical and functional properties of cowpea protein isolates treated with temperature or high hydrostatic pressure[J].Innovative Food Science & Emerging Technologies,2016,33:38-46.
[21]MU D,LI H,LI X,et al.Enhancing laccase-induced soybean protein isolates gel properties by microwave pretreatment[J].Journal of Food Processing and Preservation,2020,44(4):e14386.
[22]GUO C,WANG X,WANG Y.Dielectric properties of soy protein isolate dispersion and its temperature profile during radio frequency heating[J].Journal of Food Processing and Preservation,2018,42(7):e13659.
[23]HAN Z,CAI M J,CHENG J H,et al.Effects of electric fields and electromagnetic wave on food protein structure and functionality:A review [J].Trends in Food Science & Technology,2018,75:1-9.
[24]ZHANG X X,WANG L,CHEN Z X,et al.Effect of high energy electron beam on proteolysis and antioxidant activity of rice proteins[J].Food & Function,2020,11(1):871-882.
[25]WANG Y R,YANG Q,FAN J L,et al.The effects of phosphorylation modification on the structure,interactions and rheological properties of rice glutelin during heat treatment[J].Food Chemistry,2019,297:124978.
[26]LI T,WANG L,CHEN Z,et al.Electron beam irradiation induced aggregation behaviour,structural and functional properties changes of rice proteins and hydrolysates[J].Food Hydrocolloids,2019,97:105192.
[27]吴英.高压均质处理改善大豆7S 蛋白功能性质与输送特性研究[D].长沙:中南林业科技大学,2021.
WU Y.High pressure homogenization treatment to improve the functional properties and transport properties of soybean 7S protein[D].Changsha:Central South University of Forestry and Technology,2021.
[28]PICCINI L,SCILINGO A,SPERONI F.Thermal Versus High Hydrostatic Pressure Treatments on Calcium-added Soybean Proteins.Protein Solubility,Colloidal Stability and Cold-set Gelation[J].Food Biophysics,2019,14(1):69-79.
[29]AL-RUWAIH N,AHMED J,MULLA M F,et al.High-pressure assisted enzymatic proteolysis of kidney beans protein isolates and characterization of hydrolysates by functional,structural,rheological and antioxidant properties[J].LWT,2019,100(2):231-236.
[30]ZHANG J,LIU L,LIU H,et al.Changes in conformation and quality of vegetable protein during texturization process by extrusion[J].Critical Reviews in Food Science and Nutrition,2019,59(20):3267-3280.
[31]许英一,马鑫蕊,徐艳霞,等.不同种类糖对燕麦蛋白糖基化产物功能性质及结构的影响[J/OL].中国油脂,(2022-04-22)[2022-06-01].https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CAPJ&dbname=CAPJLAST&filename=ZYZZ20220414000&uniplatf -orm=NZKPT&v=gLnnDDeHK -LNPYyTgckkcH_f9 -gJoZiO6IOWBNsjDi-ppEhAsbkjk9Ae6C7iQyAa.
XU Y Y,MA X R,XU Y X,et al.Effects of different types of sugars on the functional properties and structures of oat protein glycosylation products[J/OL].China Oil & Fats,(2022-04-22)[2022-06-01].https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CAPJ&dbname=CAPJLAST&filename=ZYZZ20220 414000&uniplatform=NZKPT&v=gLnnDDeHK -LNPYyTgckkcH_f9 -gJoZiO6IOWBNsjDi -ppEhAsbkjk9Ae6C7iQyAa.
[32]WANG L H,SUN X,HUANG G Q,et al.Conjugation of soybean protein isolate with xylose/fructose through wet-heating Maillard reaction[J].Journal of Food Measurement and Characterization,2018,12(4):2718-2724.
[33]刘静媛,王睿粲,吕莹,等.磷酸化和糖基化对大豆蛋白体外消化性的影响[J].中国食品学报,2021,21(2):89-99.
LIU J Y,WANG R C,LV Y,et al.Effects of phosphorylation and glycosylation on in vitro digestibility of soybean protein[J].Journal of Chinese Institute of Food Science and Technology,2021,21(2):89-99.
[34]刘雯,江连洲,李杨,等.琥珀酰化对水酶法提取大豆蛋白的影响[J].大豆科技,2019,S1:258-262.
LIU W,JIANG L Z,LI Y,et al.Effects of succinylation on the extraction of soybean protein by aqueous enzymatic method[J].Soybean Science and Technology,2019,S1:258-262.
[35]周小玲,刘永乐,李向红,等.蛋白质谷氨酰胺酶对米谷蛋白的分子结构及功能性质的影响[J].中国食品学报,2010,10(5):98-105.
ZHOU X L,LIU Y L,LI X H,et al.Effects of protein glutaminase on the molecular structure and functional properties of rice glutenin[J].Journal of Chinese Institute of Food Science and Technology,2010,10(5):98-105.
[36]耿蕊,卢岩,孔保华,等.pH 偏移结合加热处理对大豆分离蛋白乳化特性的影响[J].中国食品学报,2016,16(1):173-180.
GENG R,LU Y,KONG B H,et al.Effects of pH excursion combined with heat treatment on the emulsification properties of soybean protein isolate[J].Journal of Chinese Institute of Food Science and Technology,2016,16(1):173-180.
[37]LI R,CUI Q,WANG G,et al.Relationship between surface functional properties and flexibility of soy protein isolate-glucose conjugates[J].Food Hydrocolloids,2019,95:349-357.
[38]KUTZLI I,GRIENER D,GIBIS M,et al.Influence of Maillard reaction conditions on the formation and solubility of pea protein isolate -maltodextrin conjugates in electrospun fibers[J].Food Hydrocolloids,2020,101:105535.
[39]S O CY,H M.Modified soybean protein with high water-holding capacity[J].Cereal Chemistry,1978,55(2):157-167.
[40]SANCHEZ-RESENDIZ A,RODRIGUEZ-BARRIENTOS S,RODRIGUEZ-RODRIGUEZ J,et al.Phosphoesterification of soybean and peanut proteins with sodium trimetaphosphate(STMP):Changes in structure to improve functionality for food applications[J].Food Chemistry,2018,260:299-305.
[41]SHAH N N,UMESH K V,SINGHAL R S.Hydrophobically modified pea proteins:Synthesis,characterization and evaluation as emulsifiers in eggless cake[J].Journal of Food Engineering,2019,255:15-23.
[42]HE W,YANG R,ZHAO W.Effect of acid deamidation-alcalase hydrolysis induced modification on functional and bitter -masking properties of wheat gluten hydrolysates[J].Food Chemistry,2019,277:655-663.
[43]JIANG Z Q,SONTAG-STROHM T,SALOVAARA H,et al.Oat protein solubility and emulsion properties improved by enzymatic deamidation[J].Journal of Cereal Science,2015,64:126-132.
[44]KUNARAYAKUL S,THAIPHANIT S,ANPRUNG P,et al.Optimization of coconut protein deamidation using protein-glutaminase and its effect on solubility,emulsification,and foaming properties of the proteins[J].Food Hydrocolloids,2018,79:197-207.
[45]MUNEER F,JOHANSSON E,HEDENQVIST M S,et al.Impact of pH modification on protein polymerization and structure -function relationships in potato protein and wheat gluten composites[J].International Journal of Molecular Sciences,2019,20(1):58.
[46]ZHANG W,LIU C,ZHAO J,et al.Modification of structure and functionalities of ginkgo seed proteins by pH-shifting treatment[J].Food Chemistry,2021,358:129862.
[47]ECKERT E,HAN J,SWALLOW K,et al.Effects of enzymatic hydrolysis and ultrafiltration on physicochemical and functional properties of faba bean protein[J].Cereal Chemistry,2019,96(4):725-741.
[48]MEINLSCHMIDT P,UEBERHAM E,LEHMANN J,et al.The effects of pulsed ultraviolet light,cold atmospheric pressure plasma,and gamma-irradiation on the immunoreactivity of soy protein isolate[J].Innovative Food Science & Emerging Technologies,2016,38(12):374-383.
[49]KLUPSAITE D,JUODEIKIENE G,ZADEIKE D,et al.The influence of lactic acid fermentation on functional properties of narrow-leaved lupine protein as functional additive for higher value wheat bread[J].LWT,2017,75(2):180-186.
[50]YANG X,TENG D,WANG X,et al.Enhancement of Nutritional and Antioxidant Properties of Peanut Meal by Bio -modification with Bacillus licheniformis[J].Applied Biochemistry and Biotechnology,2016,180(6):1227-1242.
[51]RUI X,HUANG J,XING G,et al.Changes in soy protein immunoglobulin E reactivity,protein degradation,and conformation through fermentation with Lactobacillus plantarum strains[J].LWT-Food Science and Technology,2019,99(2):156-165.
[52]CAO Y,MEZZENGA R.Food protein amyloid fibrils:Origin,structure,formation,characterization,applications and health implications[J].Advances in Colloid and Interface Science,2019,269(7):334-356.
[53]MOHAMMADIAN M,MADADLOU A.Technological functionality and biological properties of food protein nanofibrils formed by heating at acidic condition[J].Trends in Food Science & Technology,2018,75(5):115-128.
[54]LAMBRECHT M A,JANSENS K J A,ROMBOUTS I,et al.Conditions governing food protein amyloid fibril formation.Part II:Milk and legume proteins[J].Comprehensive Reviews in Food Science and Food Safety,2019,18(4):1277-1291.
[55]TONG X,CAO J,TIAN T,et al.Changes in structure,rheological property and antioxidant activity of soy protein isolate fibrils by ultrasound pretreatment and EGCG[J].Food Hydrocolloids,2022,122(7):107084.
[56]赵婧,宋弋,刘攀航,等.植物基替代蛋白的利用进展[J].食品工业科技,2021,42(18):8.
ZHAO J,SONG Y,LIU P H,et al.Progress in utilization of plant-based alternative proteins[J].Food Industry Science and Technology,2021,42(18):8.
[57]PIETSCH V L,WERNER R,KARBSTEIN H P,et al.High moisture extrusion of wheat gluten:Relationship between process parameters,protein polymerization,and final product characteristics[J].Journal of Food Engineering,2019,259(10):3-11.
[58]ZHANG T,DOU W,ZHANG X,et al.The development history and recent updates on soy proteinbased meat alternatives[J].Trends in Food Science &Technology,2021,109(3):702-710.
[59]DO CARMO C S,KNUTSEN S H,MALIZIA G,et al.Meat analogues from a faba bean concentrate can be generated by high moisture extrusion[J].Future Foods,2021,3(6):100014.
[60]DOU W,ZHANG X,ZHAO Y,et al.High moisture extrusion cooking on soy proteins:Importance influence of gums on promoting the fiber formation[J].Food Research International,2022,156(6):111189.
[61]窦薇,张鑫,赵煜,等.海藻酸钠添加对大豆浓缩蛋白植物肉特性的影响[J/OL].食品科学,(2021-11-03)[2022-06-01].https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CAPJ&dbname=CAPJLAST&filename=SPKX20211028000&uniplatform=NZKPT&v=3RAbDEYpQvnTenoQ59oSXNuoRPQ6vHGeAhL -uDvdZB6RukqtRn44MjH1asVF0KWc.
DOU W,ZHANG X,ZHAO Y,et al.Effects of sodium alginate supplementation on properties of soybean protein concentrate vegetable meat [J/OL].Food Science,(2021-11-03)[2022-06-01].https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CAPJ&dbname=CAPJLAST&filename=SPKX20211028000&uniplatform=NZKPT&v=3RAbDEYpQvnTenoQ59oSXNuoRPQ6vHGeAhL-uD vdZB6RukqtRn44MjH1asVF 0KWc.
[62]ZHANG X,ZHAO Y,ZHANG T,et al.High moisture extrusion of soy protein and wheat gluten blend:An underlying mechanism for the formation of fibrous structures [J].LWT,2022,163(15):113561.
[63]王强,张金闯.高水分挤压技术的研究现状、机遇及挑战[J].中国食品学报,2018,18(7):9.
WANG Q,ZHANG J C.Research status,opportunities and challenges of high moisture extrusion technology[J].Journal of Chinese Institute of Food Science and Technology,2018,18(7):9.
[64]江连洲,张鑫,窦薇,等.植物基肉制品研究进展与未来挑战[J].中国食品学报,2020,20(8):10.
JIANG L Z,ZHANG X,DOU W,et al.Research progress and future challenges of plant-based meat products[J].Journal of Chinese Institute of Food Science and Technology,2020,20(8):10.
[65]LIN S,HUFF H,HSIEH F.Extrusion process parameters,sensory characteristics,and structural properties of a high moisture soy protein meat analog[J].Journal of Food Science,2002,67(3):1066-1072.
[66]MACDONALD R S,PRYZBYSZEWSKI J,HSIEH F H.Soy protein isolate extruded with high moisture retains high nutritional quality [J].Journal of Agricul tural and Food Chemistry,2009,57(9):3550-3555.
[67]SMETANA S,LARKI N A,PERNUTZ C,et al.Structure design of insect-based meat analogs with high-moisture extrusion[J].Journal of Food Engineering,2018,229(7):83-95.
[68]ZHANG J,LIU L,ZHU S,et al.Texturisation behaviour of peanut-soy bean/wheat protein mixtures during high moisture extrusion cooking[J].International Journal of Food Science & Technology,2018,53(11):2535-2541.
[69]SILVA A R,SILVA M M,RIBEIRO B D.Health issues and technological aspects of plant-based alternative milk[J].Food Research International,2020,131(5):108972.
[70]BERNAT N,CHAFER M,RODRÍGUEZ-GARCÍA J,et al.Effect of high pressure homogenisation and heat treatment on physical properties and stability of almond and hazelnut milks[J].LWT-Food Science and Technology,2015,62(1):488-496.
[71]SALVE A R,PEGU K,ARYA S S.Comparative assessment of high-intensity ultrasound and hydrodynamic cavitation processing on physico -chemical properties and microbial inactivation of peanut milk[J].Ultrasonics Sonochemistry,2019,59:104728.
[72]MAGHSOUDLOU Y,ALAMI M,MASHKOUR M,et al.Optimization of ultrasound-assisted stabilization and formulation of almond milk[J].Journal of Food Processing and Preservation,2016,40(5):828-839.
[73]VANGA S K,WANG J,ORSAT V,et al.Effect of pulsed ultrasound,a green food processing technique,on the secondary structure and in-vitro digestibility of almond milk protein[J].Food Research International,2020,137(12):109523.
[74]TORO-FUNES N,BOSCH-FUSTÉ J,VECIANANOGUÉS M,et al.Effect of ultra high pressure homogenization treatment on the bioactive compounds of soya milk[J].Food Chemistry,2014,152(6):597-602.
[75]POLISELI-SCOPEL F H,HERNÁNDEZ-HERRERO M,GUAMIS B,et al.Comparison of ultra high pressure homogenization and conventional thermal treatments on the microbiological,physical and chemical quality of soymilk[J].LWT-Food Science and Technology,2012,46(1):42-48.
[76]VAGADIA B H,VANGA S K,SINGH A,et al.Comparison of conventional and microwave treatment on soymilk for inactivation of trypsin inhibitors and in vitro protein digestibility[J].Foods,2018,7(1):6.
[77]LI F D,CHEN C,REN J,et al.Effect of ohmic heating of soymilk on urease inactivation and kinetic analysis in holding time[J].Journal of Food Science,2015,80(2):E307-E15.
[78]佚名.人造植物蛋上市为寻找低碳植物性食品探路[J].黑龙江粮食,2014(7):2.
Artificial plant eggs are on the market as a way to find low-carbon plant-based foods[J].Heilongjiang Grain,2014(7):2.
[79]BR?CKEL U,MEIER W,WAGNER G.Product design and engineering:Formulation of gels and pastes[M]// USA:John Wiley & Sons,2013.
[80]GHARIBZAHEDI S M T,ROOHINEJAD S,GEORGE S,et al.Innovative food processing technologies on the transglutaminase functionality in protein-based food products:Trends,opportunities and drawbacks[J].Trends in Food Science & Technology,2018,75:194-205.
[81]HE R,JU X,YUAN J,et al.Antioxidant activities of rapeseed peptides produced by solid state fermentation[J].Food Research International,2012,49(1):432-438.
[82]BRANDSCH M,KNÜTTER I,BOSSE-DOENECKE E.Pharmaceutical and pharmacological importance of peptide transporters [J].Journal of Pharmacy and Pharmacology,2008,60(5):543-585.
[83]DI BERNARDINI R,RAI D K,BOLTON D,et al.Isolation,purification and characterization of antioxidant peptidic fractions from a bovine liver sarcoplasmic protein thermolysin hydrolyzate[J].Peptides,2011,32(2):388-400.
[84]SUETSUNA K,CHEN J R.Isolation and characterization of peptides with antioxidant activity derived from wheat gluten[J].Food Science and Technology Research,2002,8(3):227-230.
[85]ZHU K,ZHOU H,QIAN H.Antioxidant and free radical-scavenging activities of wheat germ protein hydrolysates(WGPH) prepared with alcalase[J].Process Biochemistry,2006,41(6):1296-1302.
[86]MANI-LÓPEZ E,PALOU E,LÓPEZ-MALO A.Legume proteins,peptides,water extracts,and crude protein extracts as antifungals for food applications[J].Trends in Food Science & Technology,2021,112:16-24.
[87]FREITAS C S,VERICIMO M A,DA SILVA M L,et al.Encrypted antimicrobial and antitumoral peptides recovered from a protein-rich soybean(Glycine max) by-product[J].Journal of Functional Foods,2019,54:187-198.
[88]PUCHALSKA P,GARCÍA M C,MARINA M L.Development of a capillary high performance liquid chromatography-ion trap-mass spectrometry method for the determination of VLIVP antihypertensive peptide in soybean crops[J].Journal of Chromatography A,2014,1338:85-91.
[89]YU J,MIKIASHVILI N,BONKU R,et al.Allergenicity,antioxidant activity and ACE-inhibitory activity of protease hydrolyzed peanut flour[J].Food Chemistry,2021,360:129992.
[90]WEN L,JIANG Y,ZHOU X,et al.Structure identification of soybean peptides and their immunomodulatory activity[J].Food Chemistry,2021,359:129970.
[91]HADIDI M,JAFARZADEH S,FOROUGH M,et al.Plant protein-based food packaging films;recent advances in fabrication,characterization,and applications[J].Trends in Food Science & Technology,2022,120:154-173.
[92]DUBEY N K,DUBEY R.Edible films and coatin gs:An update on recent advances[M]//Biopoly mer -based Formulations.Netherlands:Elsevier.2020:675-695.
[93]BOURTOOM T.Edible protein films:properties enhancement[J].International Food Research Journal,2009,16(1):1-9.
[94]ERDEM B G,KAYA S.Characterization and application of novel composite films based on soy protein isolate and sunflower oil produced using freeze drying method[J].Food Chemistry,2022,366:130709.
[95]CHENG J,CUI L.Effects of high-intensity ultrasound on the structural,optical,mechanical and physicochemical properties of pea protein isolatebased edible film [J].Ultrasonics Sonochemistry,2021,80:105809.
[96]CHENG J,LI Z,WANG J,et al.Structural characteristics of pea protein isolate(PPI) modified by high-pressure homogenization and its relation to the packaging properties of PPI edible film [J].Food Chemistry,2022,388:132974.
[97]ZHANG C,WANG Z,LI Y,et al.The preparation and physiochemical characterization of rapeseed protein hydrolysate-chitosan composite films[J].Food Chemistry,2019,272:694-701.
[98]ASSAD I,BHAT S U,GANI A,et al.Protein based packaging of plant origin:Fabrication,properties,recent advances and future perspectives[J].International Journal of Biological Macromolecules,2020,164:707-716.